Discovery and development of gliflozins/ja: Difference between revisions
Created page with "過去10年間、高血糖の発症と維持における腎臓の役割が検討されてきた。腎臓の役割は、ナトリウム/グルコーストランスポーター2タンパク質を阻害する薬物の開発につながった。健康な成人では、毎日約180グラムのグルコースが糸球体で濾過され、原尿中に失われるが、最初に濾過されたグルコースの90%以上は、近位尿細管の初期凸分節..." Tags: Mobile edit Mobile web edit |
Created page with "=== フロリジン === thumb|フロリジン フロリジンは100年以上前から知られている化合物である。天然に存在する植物性グルコシドであり、腎近位尿細管および小腸の粘膜に存在するナトリウム/グルコースシンポーターを阻害することにより、腎糖尿を生じさせ、腸の..." Tags: Mobile edit Mobile web edit |
||
| Line 28: | Line 28: | ||
過去10年間、高血糖の発症と維持における腎臓の役割が検討されてきた。腎臓の役割は、ナトリウム/グルコーストランスポーター2タンパク質を阻害する薬物の開発につながった。健康な成人では、毎日約180グラムのグルコースが[[glomeruli/ja|糸球体]]で濾過され、原尿中に失われるが、最初に濾過されたグルコースの90%以上は、近位尿細管の初期凸分節にあるSGLT-2によって制御される高容量システムによって再吸収される。残りの濾過されたグルコースはほとんどすべてナトリウム/グルコーストランスポーター1によって再吸収されるため、正常な状況下では、濾過されたグルコースはほとんどすべて再吸収され、糖尿病でない人の尿中に含まれる[[glucose/ja|グルコース]]は100 mg未満である。 | 過去10年間、高血糖の発症と維持における腎臓の役割が検討されてきた。腎臓の役割は、ナトリウム/グルコーストランスポーター2タンパク質を阻害する薬物の開発につながった。健康な成人では、毎日約180グラムのグルコースが[[glomeruli/ja|糸球体]]で濾過され、原尿中に失われるが、最初に濾過されたグルコースの90%以上は、近位尿細管の初期凸分節にあるSGLT-2によって制御される高容量システムによって再吸収される。残りの濾過されたグルコースはほとんどすべてナトリウム/グルコーストランスポーター1によって再吸収されるため、正常な状況下では、濾過されたグルコースはほとんどすべて再吸収され、糖尿病でない人の尿中に含まれる[[glucose/ja|グルコース]]は100 mg未満である。 | ||
=== フロリジン === | |||
[[File:Phlorhizin.svg|thumb|フロリジン]] | |||
[[File:Phlorhizin.svg|thumb| | [[Phlorizin/ja|フロリジン]]は100年以上前から知られている化合物である。天然に存在する植物性[[glucoside/ja|グルコシド]]であり、腎近位尿細管および[[small intestine/ja|小腸]]の粘膜に存在するナトリウム/グルコース[[Symporter/ja|シンポーター]]を阻害することにより、[[Renal glycosuria/ja|腎糖尿]]を生じさせ、腸のグルコース吸収を阻害する。フロリジンは1835年に初めて単離され、その後、SGLT-1とSGLT-2の両タンパク質に対して強力ではあるが非選択的な阻害剤であることが判明した。 | ||
[[Phlorizin]] | |||
<div lang="en" dir="ltr" class="mw-content-ltr"> | <div lang="en" dir="ltr" class="mw-content-ltr"> | ||
Revision as of 12:40, 14 February 2024
グリフロジンは、2型糖尿病(T2D)の治療薬の一種である。これらはナトリウム/グルコース共輸送体2(SGLT-2)を阻害することで作用するため、SGLT-2阻害薬とも呼ばれる。薬物の有効性は腎排泄に依存し、糖排泄を促進することでグルコースが血液循環に乗るのを防ぐ。作用機序はインスリン非依存性である。
米国では、ダパグリフロジン、カナグリフロジン、エンパグリフロジンの3つの薬物が食品医薬品局(FDA)に受け入れられている。カナグリフロジンは2013年3月にFDAに承認された最初のSGLT-2阻害薬である。ダパグリフロジンとエンパグリフロジンは2014年に承認された。
導入
グルコースホメオスタシスにおける腎臓の役割
二次活性グルコーストランスポーターであるSLC-5遺伝子ファミリーには少なくとも4つのメンバーが存在する。ナトリウムグルコーストランスポータータンパク質SGLT-1とSGLT-2は、このファミリーの2つの主要メンバーである。これら2つのメンバーは、他のトランスポーターの中でも腎臓に存在し、そこでは血糖に関連する主要な共トランスポーターである。腎臓でのグルコース再吸収と腸でのグルコース吸収に関与している。
血中グルコースは糸球体で自由に濾過され、SGLT-1とSGLT-2は腎臓でグルコースを再吸収し、循環細胞に戻す。SGLT-2は再吸収の90%を、SGLT-1は残りの10%を担っている。
SGLT-2タンパク質
ナトリウム/グルコース共輸送体(SGLT)タンパク質は細胞膜に結合しており、グルコースの濃度勾配に逆らって、グルコースを細胞膜を通して細胞内に輸送する役割を持っている。これはナトリウム/カリウムATPaseポンプによって生じるナトリウム勾配を利用することで行われるため、グルコースが細胞内に輸送されると同時にナトリウムも輸送される。勾配に逆らっているため、働くにはエネルギーが必要である。SGLTタンパク質は、インスリンとは無関係に、糸球体濾液からのグルコース再吸収を引き起こす。
SGLT-2はグルコーストランスポーターファミリーの一員であり、低親和性で高容量のグルコーストランスポーターである。SGLT-2は主に近位腎尿細管のS-1およびS-2セグメントで発現しており、濾過されたグルコースの大部分が吸収される。SGLT-2はグルコースの調節に関与し、腎臓におけるグルコースの再吸収の大部分を担っている。
糖尿病では、細胞外グルコース濃度が上昇し、この高いグルコースレベルがSGLT-2のアップレギュレーションを引き起こし、腎臓でのグルコースの吸収を増加させる。これらの作用により、高血糖が維持される。ナトリウムはSGLT-2を介してグルコースと同時に吸収されるため、SGLT-2のアップレギュレーションはおそらく高血圧の発症または維持につながる。ラットにラミプリルまたはロサルタンを与えた研究では,SGLT-2タンパク質とmRNAのレベルが有意に減少した。糖尿病患者において高血圧は一般的な問題であるため、この疾患との関連性があるかもしれない。
ナトリウム/グルコース共輸送体2を阻害する薬物は、腎のグルコース再吸収を阻害し、尿中グルコース排泄を促進し、血中グルコースを低下させる。これらの薬剤はインスリンとは独立して作用し、低血糖や体重増加を引き起こすことなくグルコースレベルを低下させることができる。
発見
中世の医師たちは日常的に尿を試飲し、その観察結果を論述していた。糖尿病は尿中にブドウ糖が排出されることから腎障害であると考えたのは当初どの医師であったかは、現在では歴史から失われているらしい。インスリンの発見は、やがて膵臓に焦点を当てた糖尿病管理につながった。糖尿病の治療戦略の伝統的な焦点は、内因性インスリン分泌の増強とインスリン感受性の改善であった。
過去10年間、高血糖の発症と維持における腎臓の役割が検討されてきた。腎臓の役割は、ナトリウム/グルコーストランスポーター2タンパク質を阻害する薬物の開発につながった。健康な成人では、毎日約180グラムのグルコースが糸球体で濾過され、原尿中に失われるが、最初に濾過されたグルコースの90%以上は、近位尿細管の初期凸分節にあるSGLT-2によって制御される高容量システムによって再吸収される。残りの濾過されたグルコースはほとんどすべてナトリウム/グルコーストランスポーター1によって再吸収されるため、正常な状況下では、濾過されたグルコースはほとんどすべて再吸収され、糖尿病でない人の尿中に含まれるグルコースは100 mg未満である。
フロリジン
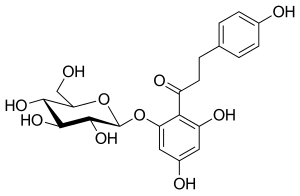
フロリジンは100年以上前から知られている化合物である。天然に存在する植物性グルコシドであり、腎近位尿細管および小腸の粘膜に存在するナトリウム/グルコースシンポーターを阻害することにより、腎糖尿を生じさせ、腸のグルコース吸収を阻害する。フロリジンは1835年に初めて単離され、その後、SGLT-1とSGLT-2の両タンパク質に対して強力ではあるが非選択的な阻害剤であることが判明した。
Phlorizin seemed to have very interesting properties and the results in animal studies were encouraging, it improved insulin sensitivity and in diabetic rat models it seemed to increase glucose levels in urine and also normal glucose concentration in plasma occurred without hypoglycemia. Unfortunately, in spite of these properties, phlorizin was not suitable enough for clinical development for several reasons. Phlorizin has very poor oral bioavailability as it is broken down in the gastrointestinal tract, so it has to be given parenterally. Phloretin, the active metabolite of phlorizin, is a potent inhibitor of facilitative glucose transporters and phlorizin seems to lead to serious adverse events in the gastrointestinal tract like diarrhea and dehydration. Because of these reasons, phlorizin was never pursued in humans.
Although phlorizin was not suitable for further clinical trials, it served an important role in the development of SGLT-2 inhibitors. It served a basis for the recognition of SGLT inhibitors with improved safety and tolerability profiles. For an example, the SGLT inhibitors are not associated with gastrointestinal adverse events and the bioavailability is much greater.
Inhibition of SGLT-2 results as better control of glucose level, lower insulin, lower blood pressure and uric acid levels and augments calorie wasting. Some data supports the hypothesis that SGLT-2 inhibition may have direct renoprotective effects. This includes actions to attenuate tubular hypertrophy and hyperfiltration associated with diabetes and to reduce the tubular toxicity of glucose. Inhibition of SGLT-2 following treatment with dapagliflozin reduces the capacity for tubular glucose reabsorption by approximately 30–50%.
Drug development
Phlorizin consists of glucose moiety and two aromatic rings (aglycone moiety) joined by an alkyl spacer. Initially, phlorizin was isolated for treatment of fever and infectious diseases, particularly malaria. According to Michael Nauck and his partners, studies were made in the 1950s on phlorizin that showed that it could block sugar transport in the kidney, small intestine, and a few other tissues. In the early 1990s, sodium/glucose cotransporter 2 was fully characterized, so the mechanism of phlorizin became of real interest. In later studies it was said that sugar-blocking effects of phlorizin was due to inhibition of the sodium/glucose cotransporter proteins.
Most of the reported SGLT-2 inhibitors are glucoside analogs that can be tracked to the o-aryl glucoside found in the nature. The problem with using o-glucosides as SGLT-2 inhibitors is instability that can be tracked to degradation by β-glucosidase in the small intestine. Because of that, o-glucosides given orally have to be prodrug esters. These prodrugs go through changes in the body leading to carbon–carbon bond between the glucose and the aglycone moiety so c-glucoside are formed from the o-glucosides. C-glucosides have a different pharmacokinetic profile than o-glucosides (e.g. half-life and duration of action) and are not degraded by the β-glucosidase. The first discovered c-glucoside was the drug dapagliflozin. Dapagliflozin was the first highly selective SGLT-2-inhibitor approved by the European Medicines Agency. All SGLT-2 inhibitors in clinical development are prodrugs that have to be converted to its active ‘A’ form for activity.
T-1095

Because Phlorizin is a nonselective inhibitor with poor oral bioavailability, a phlorizin derivative was synthesised and called T-1095. T-1095 is a methyl carbonate prodrug that is absorbed into the circulation when given orally, and is rapidly converted in the liver to the active metabolite T-1095A. By inhibiting SGLT-1 and SGLT-2, urinary glucose excretion increased in diabetic animals. T-1095 did not proceed in clinical development, probably because of the inhibition of SGLT-1 but non-selective SGLT inhibitors may also block glucose transporter 1 (GLUT-1). Because 90% of filtered glucose is reabsorbed through SGLT-2, research has focused specifically on SGLT-2. Inhibition of SGLT-1 may also lead to the genetic disease glucose-galactose malabsorption, which is characterized by severe diarrhea.
ISIS 388626
According to preliminary findings of a novel method of SGLT-2 inhibition, the antisense oligonucleotide ISIS 388626 improved plasma glucose in rodents and dogs by reducing mRNA expression in the proximal renal tubules by up to 80% when given once a week. It did not affect SGLT-1. A study results on long-term use of ISIS 388626 in non-human primates observed more than 1000 fold increase in glucosuria without any associated hypoglycemia. This increase in glucosuria can be attributed to a dose-dependent reduction in the expression of SGLT-2, where the highest dose led to more than 75% reduction. In 2011, Ionis Pharmaceuticals initiated a clinical phase 1 study with ISIS-SGLT-2RX, a 12-nucleotide antisense oligonucleotide. Results from this study were published in 2017 and the treatment was "associated with unexpected renal effects". The authors concluded that "Before the concept of antisense-mediated blocking of SGLT2 with ISIS 388626 can be explored further, more preclinical data are needed to justify further investigations."
Activity of SGLT-2 inhibitors in glycemic control
Michael Nauck recounts that meta-analyses of studies about the activity of SGLT-2 inhibitors in glycemic control in type 2 diabetes mellitus patients shows improvement in the control of glucose, when compared with placebos, metformin, sulfonylurea, thiazolidinediones, insulin and more. The HbA1c was examined after SGLT-2 inhibitors were given alone (as monotherapy) and as an add-on therapy to the other diabetes medicines. The SGLT-2 inhibitors that were used were dapagliflozin and canagliflozin and others in the same drug class. The meta-analysis was taken together from studies ranging from period of few weeks up to more than 100 weeks.
The results, summed up, were that 10 mg of dapagliflozin showed more effect than placebo in the control of glucose, when given for 24 weeks. However, no inferior efficacy of 10 mg dapagliflozin was shown when used as an add-on therapy to metformin, compared with glipizide after use for 52 weeks. 10 mg of dapagliflozin showed neither inferior efficacy compared with metformin when both of the medicines were given as monotherapy for 24 weeks.
The results from meta-analysis when canagliflozin was examined, showed that compared to a placebo, canagliflozin affects HbA1c. Meta-analysis studies also showed that 10 mg and 25 mg of empagliflozin, improved HbA1c compared with a placebo.
Structure-activity relationship (SAR)
The aglycones of both phlorizin and dapagliflozin have weak inhibition effects on SGLT-1 and SGLT-2. Two synergistic forces are involved in binding of inhibitors to SGLTs. Different sugars on the aglycone will affect and change the orientation of it in the access vestibule because one of the forces involved in the binding is the binding of sugar to the glucose site. The other force is the binding of the aglycone, which affects the binding affinity of the entire inhibitor.
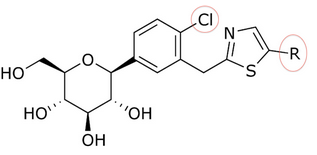
The discovery of T-1095 led to an investigation of how to enhance potency, selectivity and oral bioavailability by adding various substituents to the glycoside core. As an example we can take the change of o-glycosides to c-glycosides by creating a carbon–carbon bond between the glucose and the aglycone moiety. C-glucosides are more stable than o-glucosides which leads to modified half-life and duration of action. These modifications have also led to more specificity to SGLT-2. C-glucosides that have heterocyclic ring at the distal ring or proximal ring are better when it comes to anti-diabetic effect and physicochemical features all together. C-glucoside bearing thiazole at the distal ring on canagliflozin has shown good physicochemical properties that can lead to a clinical development, but still has the same anti-diabetic activity as dapagliflozin, as shown in tables 1 and 2.
Song and his partners did preparate thiazole compound by starting with carboxyl acid. Working with that, it took them three steps to get a compound like dapagliflozin with a thiazole ring. Inhibitory effects on SGLT-2 of the compounds were tested by Song and his partners. In tables 1, 2, and 3, the IC50 value changes depending on what compound is in the ring position, in the C-4 region of the proximal phenyl ring, and how the thiazole ring relates.
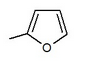
Many compounds gave different IC50 value in the ring position in an in vitro activity. For an example there was a big difference if there was an n-pentyl group (IC50 = 13,3 nM), n-butyl (IC50 = 119 nM), phenyl with 2-furyl (IC50 = 0,720) or 3-thiophenyl (IC50 = 0,772). As seen in table 1, the in vitro activity increases depending on what compound is bonded to the distal ring (given that in the C-4 region of the proximal phenyl ring is a Cl atom).
Table 1: Differences in in vitro activity depending on which compound is bonded to the distal ring.
*comparator to ethyl group (IC50 = 16,7)
In table 2, the in vitro activity changes depending on the compound in the C-4 region of the proximal phenyl ring (X). Small methyl groups or other halogen atoms in the C-4 position gave IC50 ranging from 0.72–36.7 (given that the phenyl with 2-furyl is in the ring position).
Table 2: Differences in in vitro activity depending on what compound is in the C-4 region of the proximal phenyl ring.
| X | IC50 (nM) |
|---|---|
| Cl | 0.720 |
| Me | 1.43 |
| F | 6.11 |
| H | 22.6 |
| CN | 36.7 |
Table 3: Difference in the IC50 value depending on how the thiazole ring relates (nothing else is changed in the structure (X = Cl, R = phenyl with 2-furyl).
| Compound | IC50 (nM) |
|---|---|
 |
0.720 |
 |
1.11 |
See also
| この記事は、クリエイティブ・コモンズ・表示・継承ライセンス3.0のもとで公表されたウィキペディアの項目Discovery and development of gliflozins/ja(29 August 2023編集記事参照)を素材として二次利用しています。 Lua error in Module:Itemnumber at line 91: attempt to concatenate local 'qid' (a nil value). |