コレカルシフェロール
Cholecalciferol/ja
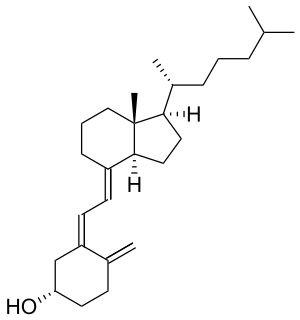
ビタミンD3としても知られるコレカルシフェロールは、日光に当たると皮膚で作られるビタミンDの一種であり、いくつかの食品に含まれており、栄養補助食品として摂取することもできる。
 | |
 | |
| Clinical data | |
|---|---|
| Pronunciation | /ˌkoʊləkælˈsɪfərɒl/ |
| Other names | vitamin D3, calciol, activated 7-dehydrocholesterol |
| AHFS/Drugs.com | Professional Drug Facts |
| License data | |
| Routes of administration | By mouth, intramuscular |
| ATC code | |
| Legal status | |
| Legal status | |
| Identifiers | |
| |
| CAS Number | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Chemical and physical data | |
| Formula | C27H44O |
| Molar mass | 384.648 g·mol−1 |
| 3D model (JSmol) | |
| Melting point | 83 to 86 °C (181 to 187 °F) |
| Boiling point | 496.4 °C (925.5 °F) |
| Solubility in water | Practically insoluble in water, freely soluble in ethanol, methanol and some other organic solvents. Slightly soluble in vegetable oils. |
| |
| |
コレカルシフェロールは、UVB光曝露後の皮膚で作られる。肝臓でカルシフェジオール(25-ヒドロキシビタミンD)に変換され、腎臓でカルシトリオール(1,25-ジヒドロキシビタミンD)に変換される。一部の魚、牛レバー、卵、チーズなどの食品に含まれる。植物、牛乳、フルーツジュース、ヨーグルト、マーガリンにも、アメリカを含む一部の国ではコレカルシフェロールが添加されていることがある。
コレカルシフェロールは、ビタミンD欠乏症を予防するための経口栄養補助食品として、またはくる病などの関連疾患を治療するための医薬品として服用することができる。また、家族性低リン血症、低血中カルシウムを引き起こしている副甲状腺機能低下症、ファンコニー症候群にも用いられる。ビタミンDサプリメントは、重度の腎臓病の人には効果がないことがある。ヒトでの過剰摂取は、嘔吐、便秘、衰弱、錯乱を引き起こすことがある。その他のリスクとしては腎臓結石がある。一般に、高血中カルシウムが起こる前に、1日あたり40,000 IU(1,000 μg)を超える用量が必要とされる。通常量である1日800~2000IUは、妊娠中でも安全である。
コレカルシフェロールは1936年に初めて記載された。世界保健機関の必須医薬品リストに掲載されている。2021年には、10 万以上の処方で、米国で65番目によく処方される医薬品であった。コレカルシフェロールはジェネリック医薬品および市販薬として入手可能である。
医薬用途
コレカルシフェロールは、ビタミンD2とは異なり、細菌やウイルスから身体を守るインターフェロンI型シグナル伝達システムを刺激するようである。
ビタミンD欠乏症
コレカルシフェロールは、皮膚で自然に合成されるビタミンDの一種で、プロホルモンとして機能し、カルシトリオールに変換される。これは、カルシウム濃度を維持し、骨の健康と発育を促進するために重要である。医薬品として、コレカルシフェロールはビタミンD欠乏症の予防や治療のために栄養補助食品として摂取されることがある。1グラムは40,000,000(40x106)IUであり、等価的に1IUは0.025 μgまたは25ngである。ビタミンD(D2であるエルゴカルシフェロールおよび/またはD3であるコレカルシフェロール)の食事摂取基準値が設定されており、推奨値は国によって異なる:
- 米国では 米国では、1歳から70歳までのすべての人(男性、女性、妊娠中・授乳中の女性)に対して、15 μg/日(600IU/日)である。70歳以上では、20 μg/日(800IU/日)が推奨されている。
- EUでは EUでは、1歳以上のすべての人に15 μg/日(600IU/日)、7~11ヵ月の乳児には10 μg/日(400IU/日)を推奨している。
- 英国では、「安全摂取量」(SI)は8. 1歳未満の乳児(母乳のみで育てられた乳児を含む)は5~10 μg/日(30~400IU/日)、1~4歳未満の小児は10 μg/日(400IU/日)、4歳以上のその他の集団(妊娠中・授乳中の女性を含む)は10 μg/日(400IU/日)の基準栄養摂取量(RNI)である。
ビタミンD濃度が低いのは、北半球の緯度に住んでいる人や、家にいる人、体が弱い人、高齢者、肥満の人、肌が黒い人、肌の大部分を覆う服を着ている人など、日光浴を定期的にしていない人によく見られる。このような人々にはサプリメントが推奨される。
2010年のInstitute of Medicineでは、ビタミンDの最大摂取量は4,000 IU/日を推奨し、最も副作用が少ない用量は1日40,000 IUを12週間以上摂取することであり、1日10,000 IU以上を7年以上摂取して毒性を示した症例は1例であるとしている。この毒性症例は、他の研究者がビタミンD摂取推奨の際に考慮すべき症例として異論を唱えている状況下で発生したものである。重度のビタミンD欠乏症の患者には負荷量による治療が必要である。その量は実際の血清25-ヒドロキシビタミンD値と体重から計算できる。
コレカルシフェロール(D3)とエルゴカルシフェロール(D2)の相対的な有効性については相反する報告があり、D2の有効性が低いとする研究もあれば、差がないとする研究もある。2つの型の吸収、結合、不活性化には違いがあり、血中濃度を上げるには通常コレカルシフェロールに有利な証拠があるが、さらなる研究が必要である。
くる病におけるコレカルシフェロール療法のあまり一般的でない使用法は、1回の大量投与であり、ストス療法と呼ばれている。治療は、経口または筋肉内注射で、300,000IU(7,500 μg)~500,000IU(12,500 μg=12.5 mg)を単回投与するか、場合によっては2~4回に分けて投与する。このような大量投与の安全性については懸念がある。
循環ビタミンD濃度が低いことは、男性の総テストステロン濃度の低下と関連している。ビタミンDの補充は総テストステロン濃度を改善する可能性があるが、さらなる研究が必要である。
その他の疾患
2007年のメタアナリシスでは、ビタミンD3を1日あたり1000~2000IU摂取することで、大腸がんの発生率を最小限のリスクで減少させることができると結論づけている。また、2008年にCancer Research誌に発表された研究では、1日1000IUのコレカルシフェロールを摂取させた新しい欧米食と同様の栄養組成のマウスに、ビタミンD3を(カルシウムとともに)添加したところ、大腸がんの発生が抑制されたことが示されている。ヒトでは、1日400IUのコレカルシフェロールサプリメントでは、大腸癌のリスクに対する影響は見られなかった。
Supplements are not recommended for prevention of cancer as any effects of cholecalciferol are very small. Although correlations exist between low levels of blood serum cholecalciferol and higher rates of various cancers, multiple sclerosis, tuberculosis, heart disease, and diabetes, the consensus is that supplementing levels is not beneficial. It is thought that tuberculosis may result in lower levels. It, however, is not entirely clear how the two are related.
Biochemistry
Structure
Cholecalciferol is one of the five forms of vitamin D. Cholecalciferol is a secosteroid, that is, a steroid molecule with one ring open.
Mechanism of action
By itself cholecalciferol is inactive. It is converted to its active form by two hydroxylations: the first in the liver, by CYP2R1 or CYP27A1, to form 25-hydroxycholecalciferol (calcifediol, 25-OH vitamin D3). The second hydroxylation occurs mainly in the kidney through the action of CYP27B1 to convert 25-OH vitamin D3 into 1,25-dihydroxycholecalciferol (calcitriol, 1,25-(OH)2vitamin D3). All these metabolites are bound in blood to the vitamin D-binding protein. The action of calcitriol is mediated by the vitamin D receptor, a nuclear receptor which regulates the synthesis of hundreds of proteins and is present in virtually every cell in the body.
Biosynthesis
Click on icon in lower right corner to open.
Click on genes, proteins and metabolites below to link to respective articles. [§ 1]
- ↑ The interactive pathway map can be edited at WikiPathways: "VitaminDSynthesis_WP1531".
7-Dehydrocholesterol is the precursor of cholecalciferol. Within the epidermal layer of skin, 7-dehydrocholesterol undergoes an electrocyclic reaction as a result of UVB light at wavelengths between 290 and 315 nm, with peak synthesis occurring between 295 and 300 nm. This results in the opening of the vitamin precursor B-ring through a conrotatory pathway making previtamin D3 (pre-cholecalciferol). In a process which is independent of UV light, the pre-cholecalciferol then undergoes a [1,7] antarafacial sigmatropic rearrangement and therein finally isomerizes to form vitamin D3.
The active UVB wavelengths are present in sunlight, and sufficient amounts of cholecalciferol can be produced with moderate exposure of the skin, depending on the strength of the sun. Time of day, season, latitude, and altitude affect the strength of the sun, and pollution, cloud cover or glass all reduce the amount of UVB exposure. Exposure of face, arms and legs, averaging 5–30 minutes twice per week, may be sufficient, but the darker the skin, and the weaker the sunlight, the more minutes of exposure are needed. Vitamin D overdose is impossible from UV exposure; the skin reaches an equilibrium where the vitamin degrades as fast as it is created.
Cholecalciferol can be produced in skin from the light emitted by the UV lamps in tanning beds, which produce ultraviolet primarily in the UVA spectrum, but typically produce 4% to 10% of the total UV emissions as UVB. Levels in blood are higher in frequent users of tanning salons.
Whether cholecalciferol and all forms of vitamin D are by definition "vitamins" can be disputed, since the definition of vitamins includes that the substance cannot be synthesized by the body and must be ingested. Cholecalciferol is synthesized by the body during UVB radiation exposure.
The three steps in the synthesis and activation of vitamin D3 are regulated as follows:
- Cholecalciferol is synthesized in the skin from 7-dehydrocholesterol under the action of ultraviolet B (UVB) light. It reaches an equilibrium after several minutes depending on the intensity of the UVB in the sunlight – determined by latitude, season, cloud cover, and altitude – and the age and degree of pigmentation of the skin.
- Hydroxylation in the endoplasmic reticulum of liver hepatocytes of cholecalciferol to calcifediol (25-hydroxycholecalciferol) by 25-hydroxylase is loosely regulated, if at all, and blood levels of this molecule largely reflect the amount of cholecalciferol produced in the skin combined with any vitamin D2 or D3 ingested.
- Hydroxylation in the kidneys of calcifediol to calcitriol by 1-alpha-hydroxylase is tightly regulated: it is stimulated by parathyroid hormone and serves as the major control point in the production of the active circulating hormone calcitriol (1,25-dihydroxyvitamin D3).
Industrial production
Cholecalciferol is produced industrially for use in vitamin supplements and to fortify foods. As a pharmaceutical drug it is called cholecalciferol (USAN) or colecalciferol (INN, BAN). It is produced by the ultraviolet irradiation of 7-dehydrocholesterol extracted from lanolin found in sheep's wool. Cholesterol is extracted from wool grease and wool wax alcohols obtained from the cleaning of wool after shearing. The cholesterol undergoes a four-step process to make 7-dehydrocholesterol, the same compound that is produced in the skin of animals. The 7-dehydrocholesterol is then irradiated with ultraviolet light. Some unwanted isomers are formed during irradiation: these are removed by various techniques, leaving a resin which melts at about room temperature and usually has a potency of 25,000,000 to 30,000,000 International Units per gram.
Cholecalciferol is also produced industrially for use in vitamin supplements from lichens, which is suitable for vegans.
Stability
Cholecalciferol is very sensitive to UV radiation and will rapidly, but reversibly, break down to form supra-sterols, which can further irreversibly convert to ergosterol.
Pesticide
Rodents are somewhat more susceptible to high doses than other species, and cholecalciferol has been used in poison bait for the control of these pests.
The mechanism of high dose cholecalciferol is that it can produce "hypercalcemia, which results in systemic calcification of soft tissue, leading to kidney failure, cardiac abnormalities, hypertension, CNS depression, and GI upset. Signs generally develop within 18-36 hr of ingestion and can include depression, loss of appetite, polyuria, and polydipsia." High-dose cholecalciferol will tend to rapidly accumulate in adipose tissue yet release more slowly which will tend to delay time of death for several days from the time that high-dose bait is introduced.
In New Zealand, possums have become a significant pest animal. For possum control, cholecalciferol has been used as the active ingredient in lethal baits. The LD50 is 16.8 mg/kg, but only 9.8 mg/kg if calcium carbonate is added to the bait. Kidneys and heart are target organs. LD50 of 4.4 mg/kg has been reported in rabbits, with lethality to almost all rabbits ingesting doses greater than 15 mg/kg. Toxicity has been reported across a wide range of cholecalciferol dosages, with LD50 as high as 88 mg/kg or LDLo as low as 2 mg/kg reported for dogs.
Researchers have reported that the compound is less toxic to non-target species than earlier generations of anticoagulant rodenticides (Warfarin and congeners) or Bromethalin, and that relay toxicosis (poisoning by eating a poisoned animal) has not been documented. Nevertheless, the same source reports that use of cholecalciferol in rodenticides may still pose a significant hazard to other animals, such as dogs and cats, when rodenticide bait or other forms of cholecalciferol are directly ingested.
こちらも参照
- Hypervitaminosis D/ja, ビタミンD中毒
- エルゴカルシフェロール, ビタミンD2
- 25-Hydroxyvitamin D 1-alpha-hydroxylase/ja, カルシフェジオールをカルシトリオールに変換する腎臓の酵素である。