Potassium/ja: Difference between revisions
Created page with "===化合物=== thumb|left|upright|固体スーパーオキシドカリウム({{chem2|KO2}})の構造" |
|||
| Line 32: | Line 32: | ||
[[Image:potassium-superoxide-unit-cell-3D-ionic.png|thumb|left|upright|固体スーパーオキシドカリウム({{chem2|KO2}})の構造]] | [[Image:potassium-superoxide-unit-cell-3D-ionic.png|thumb|left|upright|固体スーパーオキシドカリウム({{chem2|KO2}})の構造]] | ||
[[potassium oxide/ja|酸化カリウム]]({{chem2|K2O}})、過酸化カリウム({{chem2|K2O2}})、過酸化カリウム({{chem2|KO2}})、オゾン化カリウム({{chem2|KO3}})である。カリウムと酸素の二元化合物は、水と反応してKOHを形成する。 | |||
<div lang="en" dir="ltr" class="mw-content-ltr"> | <div lang="en" dir="ltr" class="mw-content-ltr"> | ||
Revision as of 10:48, 22 April 2024
Page Template:Infobox element/styles.css has no content.
 Potassium pearls (in paraffin oil, ~5 mm each) | ||||||||||||||||||||||||||||||
| Potassium | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Appearance | silvery white, faint bluish-purple hue when exposed to air | |||||||||||||||||||||||||||||
| Standard atomic weight Ar°(K) | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
| Potassium in the periodic table | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
| Atomic number (Z) | 19 | |||||||||||||||||||||||||||||
| Electron configuration | [Ar] 4s1 | |||||||||||||||||||||||||||||
| Electrons per shell | 2, 8, 8, 1 | |||||||||||||||||||||||||||||
| Physical properties | ||||||||||||||||||||||||||||||
| Phase at STP | solid | |||||||||||||||||||||||||||||
| Melting point | 336.7 K (63.5 °C, 146.3 °F) | |||||||||||||||||||||||||||||
| Boiling point | 1030.793 K (757.643 °C, 1395.757 °F) | |||||||||||||||||||||||||||||
| Density (at 20° C) | 0.8590 g/cm3 | |||||||||||||||||||||||||||||
| when liquid (at m.p.) | 0.82948 g/cm3 | |||||||||||||||||||||||||||||
| Critical point | 2223 K, 16 MPa | |||||||||||||||||||||||||||||
| Heat of fusion | 2.33 kJ/mol | |||||||||||||||||||||||||||||
| Heat of vaporization | 76.9 kJ/mol | |||||||||||||||||||||||||||||
| Molar heat capacity | 29.6 J/(mol·K) | |||||||||||||||||||||||||||||
| Atomic properties | ||||||||||||||||||||||||||||||
| Oxidation states | −1, +1 (a strongly basic oxide) | |||||||||||||||||||||||||||||
| Electronegativity | Pauling scale: 0.82 | |||||||||||||||||||||||||||||
| Ionization energies |
| |||||||||||||||||||||||||||||
| Atomic radius | empirical: 227 pm | |||||||||||||||||||||||||||||
| Covalent radius | 203±12 pm | |||||||||||||||||||||||||||||
| Van der Waals radius | 275 pm | |||||||||||||||||||||||||||||
 | ||||||||||||||||||||||||||||||
| Other properties | ||||||||||||||||||||||||||||||
| Natural occurrence | primordial | |||||||||||||||||||||||||||||
| Crystal structure | body-centered cubic (bcc) (cI2) | |||||||||||||||||||||||||||||
| Lattice constant | a = 532.69 pm (at 20 °C) | |||||||||||||||||||||||||||||
| Thermal expansion | 77.37×10−6/K (at 20 °C) | |||||||||||||||||||||||||||||
| Thermal conductivity | 102.5 W/(m⋅K) | |||||||||||||||||||||||||||||
| Electrical resistivity | 72 nΩ⋅m (at 20 °C) | |||||||||||||||||||||||||||||
| Magnetic ordering | paramagnetic | |||||||||||||||||||||||||||||
| Molar magnetic susceptibility | +20.8×10−6 cm3/mol (298 K) | |||||||||||||||||||||||||||||
| Young's modulus | 3.53 GPa | |||||||||||||||||||||||||||||
| Shear modulus | 1.3 GPa | |||||||||||||||||||||||||||||
| Bulk modulus | 3.1 GPa | |||||||||||||||||||||||||||||
| Speed of sound thin rod | 2000 m/s (at 20 °C) | |||||||||||||||||||||||||||||
| Mohs hardness | 0.4 | |||||||||||||||||||||||||||||
| Brinell hardness | 0.363 MPa | |||||||||||||||||||||||||||||
| CAS Number | 7440-09-7 | |||||||||||||||||||||||||||||
| History | ||||||||||||||||||||||||||||||
| Discovery and first isolation | Humphry Davy (1807) | |||||||||||||||||||||||||||||
| Symbol | "K": from New Latin kalium | |||||||||||||||||||||||||||||
| Isotopes of potassium | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
カリウムは化学元素の一つであり、記号はK(新ラテン語kaliumから)、原子番号 は19である。銀白色の金属で、ナイフで簡単に切れるほど柔らかい。金属カリウムは大気中の酸素と急速に反応し、わずか数秒の暴露で薄片状の白い過酸化カリウムを形成する。カリウムは植物の灰であるカリから初めて単離された。周期表では、カリウムはアルカリ金属の1つであり、すべての金属は外側の電子殻に1個の価電子を持ち、この価電子は容易に除去されて正電荷を持つイオン(陰イオンと結合して塩を形成する)を作る。自然界では、カリウムはイオン塩でのみ存在する。元素のカリウムは水と激しく反応し、反応で放出される水素に引火するのに十分な熱を発生し、薄紫色の色のついた炎で燃焼する。カリウムは花崗岩や他の火成岩の一般的な成分である斜長石など、多くの鉱物に含まれている。
カリウムはナトリウムと化学的に非常によく似ている。周期表の1族の前の元素である。両者は最初のイオン化エネルギーが似ており、各原子が唯一の外側の電子を手放すことができる。1702年に初めて、それらは同じ陰イオンと結合して類似の塩を作る別個の元素であることが示唆され、1807年に元素カリウムが初めて電気分解によって単離されたときに実証された。天然に存在するカリウムは3つの同位体から構成されており、そのうち40
Kは放射性である。40
Kの痕跡はすべてのカリウムに含まれており、人体で最も一般的な放射性同位体である。
カリウムイオンは、すべての生きた細胞の機能に不可欠である。神経細胞膜を介したカリウムイオンの移動は、正常な神経伝達に必要である。カリウムの欠乏と過剰はそれぞれ、心臓のリズム異常や様々な心電図異常など、多くの徴候や症状を引き起こす。新鮮な果物や野菜は、カリウムのよい食事源である。身体は、カリウムを細胞外から細胞内に移動させ、腎臓からのカリウム排泄を増加させることによって、血清カリウム濃度を上昇させる食事性カリウムの流入に反応する。
カリウムの工業的用途のほとんどは、塩水石鹸のような水に対するカリウム化合物の高い溶解性を利用したものである。農作物の大量生産は土壌のカリウムを急速に枯渇させるが、これはカリウムを含む農業用肥料で改善することができ、世界のカリウム化学生産の95%を占めている。
語源
カリウムの英語名はpotashという語に由来する。これは、様々なカリウム塩を抽出する初期の方法を指しており、'potに灰(ash)を入れ、水を加えて加熱し、溶液を蒸発させるというものである。1807年にハンフリー・デイヴィーが初めて電気分解を用いて純粋な元素を単離したとき、彼はそれをpotashという語に由来するpotassiumと命名した。
記号Kはkaliに由来し、語源はアルカリ(alkali)であり、alkaliはArabic: القَلْيَه「植物の灰」に由来する。1797年、ドイツの化学者マルティン・クラプロスが鉱物リューサイトとレピドライトの中に「kali」を発見し、「kali」は植物の成長の産物ではなく、実際には新しい元素を含んでいることに気づき、それをkaliと呼ぶことを提案した。1807年、ハンフリー・デイヴィは電気分解によってこの元素を生成した。1809年、ルートヴィヒ・ヴィルヘルム・ジルベルトはデイヴィの「カリウム」にKaliumという名称を提案した。1814年、スウェーデンの化学者ヨンス・ヤコブ・ベルゼリウスは化学記号Kでカリウムをkaliumと呼ぶことを提唱した。
英語圏とフランス語圏ではデイヴィとフランスの化学者ジョセフ・ルイ・ゲイ=リュサックとルイ・ジャック・テナールが好んだカリウムという名称が採用され、他のゲルマン諸国ではギルバートとクラプロスのカリウムという名称が採用された。国際純正・応用化学連合の「ゴールドブック」では、公式の化学記号をKと定めている。
特性
物理的

カリウムはリチウムに次いで密度の低い金属である。融点が低く柔らかい固体であり、ナイフで簡単に切ることができる。カリウムの外観は銀色であるが、空気に触れるとすぐに灰色に変色し始める。火炎試験では、カリウムとその化合物は766.5ナノメートルに発光ピーク波長を持つライラック色を発する。
中性のカリウム原子は19個の電子を持ち、希ガスアルゴンの配置よりも1個多い。最初のイオン化エネルギーが418.8 kJ/molと低いため、カリウム原子は最後の電子を失って正電荷を帯びる可能性が高いが、負電荷を帯びたアルカリドK−
イオンも不可能ではない。対照的に、第二イオン化エネルギーは非常に高い(3052 kJ/mol)。
化学的
カリウムは空気中の酸素、水、二酸化炭素成分と反応する。酸素とは過酸化カリウムを形成する。水とカリウムは水酸化カリウム(KOH)を形成する。カリウムと水の反応は激しく発熱することがあり、特に共生した水素ガスが発火することがある。このため、カリウムと液体のナトリウム-カリウム(NaK)合金は強力な乾燥剤であるが、現在ではそのように使用されることはない。
化合物
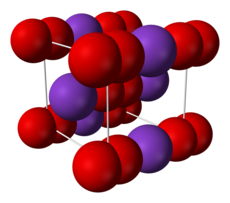
2)の構造
酸化カリウム(K
2O)、過酸化カリウム(K
2O
2)、過酸化カリウム(KO
2)、オゾン化カリウム(KO
3)である。カリウムと酸素の二元化合物は、水と反応してKOHを形成する。
KOH is a strong base. Illustrating its hydrophilic character, as much as 1.21 kg of KOH can dissolve in a single liter of water. Anhydrous KOH is rarely encountered. KOH reacts readily with carbon dioxide (CO
2) to produce potassium carbonate (K
2CO
3), and in principle could be used to remove traces of the gas from air. Like the closely related sodium hydroxide, KOH reacts with fats to produce soaps.
In general, potassium compounds are ionic and, owing to the high hydration energy of the K+
ion, have excellent water solubility. The main species in water solution are the aquo complexes [K(H
2O)
n]+
where n = 6 and 7.
Potassium heptafluorotantalate (K
2[TaF
7]) is an intermediate in the purification of tantalum from the otherwise persistent contaminant of niobium.
Organopotassium compounds illustrate nonionic compounds of potassium. They feature highly polar covalent K–C bonds. Examples include benzyl potassium KCH
2C
6H
5. Potassium intercalates into graphite to give a variety of graphite intercalation compounds, including KC
8.
Isotopes
There are 25 known isotopes of potassium, three of which occur naturally: 39
K (93.3%), 40
K (0.0117%), and 41
K (6.7%) (by mole fraction). Naturally occurring 40
K has a half-life of 1.250×109 years. It decays to stable 40
Ar by electron capture or positron emission (11.2%) or to stable 40
Ca by beta decay (88.8%). The decay of 40
K to 40
Ar is the basis of a common method for dating rocks. The conventional K-Ar dating method depends on the assumption that the rocks contained no argon at the time of formation and that all the subsequent radiogenic argon (40
Ar) was quantitatively retained. Minerals are dated by measurement of the concentration of potassium and the amount of radiogenic 40
Ar that has accumulated. The minerals best suited for dating include biotite, muscovite, metamorphic hornblende, and volcanic feldspar; whole rock samples from volcanic flows and shallow instrusives can also be dated if they are unaltered. Apart from dating, potassium isotopes have been used as tracers in studies of weathering and for nutrient cycling studies because potassium is a macronutrient required for life on Earth.
40
K occurs in natural potassium (and thus in some commercial salt substitutes) in sufficient quantity that large bags of those substitutes can be used as a radioactive source for classroom demonstrations. 40
K is the radioisotope with the largest abundance in the human body. In healthy animals and people, 40
K represents the largest source of radioactivity, greater even than 14
C. In a human body of 70 kg, about 4,400 nuclei of 40
K decay per second. The activity of natural potassium is 31 Bq/g.
History
Potash
Potash is primarily a mixture of potassium salts because plants have little or no sodium content, and the rest of a plant's major mineral content consists of calcium salts of relatively low solubility in water. While potash has been used since ancient times, its composition was not understood. Georg Ernst Stahl obtained experimental evidence that led him to suggest the fundamental difference of sodium and potassium salts in 1702, The exact chemical composition of potassium and sodium compounds, and the status as chemical element of potassium and sodium, was not known then, and thus Antoine Lavoisier did not include the alkali in his list of chemical elements in 1789. For a long time the only significant applications for potash were the production of glass, bleach, soap and gunpowder as potassium nitrate. Potassium soaps from animal fats and vegetable oils were especially prized because they tend to be more water-soluble and of softer texture, and are therefore known as soft soaps. The discovery by Justus Liebig in 1840 that potassium is a necessary element for plants and that most types of soil lack potassium caused a steep rise in demand for potassium salts. Wood-ash from fir trees was initially used as a potassium salt source for fertilizer, but, with the discovery in 1868 of mineral deposits containing potassium chloride near Staßfurt, Germany, the production of potassium-containing fertilizers began at an industrial scale. Other potash deposits were discovered, and by the 1960s Canada became the dominant producer.
Potassium metal was first isolated in 1807 by Humphry Davy, who derived it by electrolysis of molten caustic potash (KOH) with the newly discovered voltaic pile. Potassium was the first metal that was isolated by electrolysis. Later in the same year, Davy reported extraction of the metal sodium from a mineral derivative (caustic soda, NaOH, or lye) rather than a plant salt, by a similar technique, demonstrating that the elements, and thus the salts, are different. Although the production of potassium and sodium metal should have shown that both are elements, it took some time before this view was universally accepted.
Because of the sensitivity of potassium to water and air, air-free techniques are normally employed for handling the element. It is unreactive toward nitrogen and saturated hydrocarbons such as mineral oil or kerosene. It readily dissolves in liquid ammonia, up to 480 g per 1000 g of ammonia at 0 °C. Depending on the concentration, the ammonia solutions are blue to yellow, and their electrical conductivity is similar to that of liquid metals. Potassium slowly reacts with ammonia to form KNH
2, but this reaction is accelerated by minute amounts of transition metal salts. Because it can reduce the salts to the metal, potassium is often used as the reductant in the preparation of finely divided metals from their salts by the Rieke method. Illustrative is the preparation of magnesium:
- MgCl
2 + 2 K → Mg + 2 KCl
Occurrence

Potassium is formed in supernovae by nucleosynthesis from lighter atoms. Potassium is principally created in Type II supernovae via an explosive oxygen-burning process. These are nuclear fusion reactions, not to be confused with chemical burning of potassium in oxygen. 40
K is also formed in s-process nucleosynthesis and the neon burning process.
Potassium is the 20th most abundant element in the solar system and the 17th most abundant element by weight in the Earth. It makes up about 2.6% of the weight of the Earth's crust and is the seventh most abundant element in the crust. The potassium concentration in seawater is 0.39 g/L (0.039 wt/v%), about one twenty-seventh the concentration of sodium.
Geology
Elemental potassium does not occur in nature because of its high reactivity. It reacts violently with water and also reacts with oxygen. Orthoclase (potassium feldspar) is a common rock-forming mineral. Granite for example contains 5% potassium, which is well above the average in the Earth's crust. Sylvite (KCl), carnallite (KCl·MgCl
2·6H2O), kainite (MgSO
4·KCl·3H2O) and langbeinite (MgSO
4·K
2SO
4) are the minerals found in large evaporite deposits worldwide. The deposits often show layers starting with the least soluble at the bottom and the most soluble on top. Deposits of niter (potassium nitrate) are formed by decomposition of organic material in contact with atmosphere, mostly in caves; because of the good water solubility of niter the formation of larger deposits requires special environmental conditions.
Commercial production
Mining


Potassium salts such as carnallite, langbeinite, polyhalite, and sylvite form extensive evaporite deposits in ancient lake bottoms and seabeds, making extraction of potassium salts in these environments commercially viable. The principal source of potassium – potash – is mined in Canada, Russia, Belarus, Kazakhstan, Germany, Israel, the U.S., Jordan, and other places around the world. The first mined deposits were located near Staßfurt, Germany, but the deposits span from Great Britain over Germany into Poland. They are located in the Zechstein and were deposited in the Middle to Late Permian. The largest deposits ever found lie 1,000 meters (3,300 feet) below the surface of the Canadian province of Saskatchewan. The deposits are located in the Elk Point Group produced in the Middle Devonian. Saskatchewan, where several large mines have operated since the 1960s pioneered the technique of freezing of wet sands (the Blairmore formation) to drive mine shafts through them. The main potash mining company in Saskatchewan until its merge was the Potash Corporation of Saskatchewan, now Nutrien. The water of the Dead Sea is used by Israel and Jordan as a source of potash, while the concentration in normal oceans is too low for commercial production at current prices.
Chemical extraction
Several methods are used to separate potassium salts from sodium and magnesium compounds. The most-used method is fractional precipitation using the solubility differences of the salts. Electrostatic separation of the ground salt mixture is also used in some mines. The resulting sodium and magnesium waste is either stored underground or piled up in slag heaps. Most of the mined potassium mineral ends up as potassium chloride after processing. The mineral industry refers to potassium chloride either as potash, muriate of potash, or simply MOP.
Pure potassium metal can be isolated by electrolysis of its hydroxide in a process that has changed little since it was first used by Humphry Davy in 1807. Although the electrolysis process was developed and used in industrial scale in the 1920s, the thermal method by reacting sodium with potassium chloride in a chemical equilibrium reaction became the dominant method in the 1950s.
- Na + KCl → NaCl + K
The production of sodium potassium alloys is accomplished by changing the reaction time and the amount of sodium used in the reaction. The Griesheimer process employing the reaction of potassium fluoride with calcium carbide was also used to produce potassium.
- 2 KF + CaC
2 → 2 K + CaF
2 + 2 C
Reagent-grade potassium metal costs about $10.00/pound ($22/kg) in 2010 when purchased by the tonne. Lower purity metal is considerably cheaper. The market is volatile because long-term storage of the metal is difficult. It must be stored in a dry inert gas atmosphere or anhydrous mineral oil to prevent the formation of a surface layer of potassium superoxide, a pressure-sensitive explosive that detonates when scratched. The resulting explosion often starts a fire difficult to extinguish.
Cation identification
Potassium is now quantified by ionization techniques, but at one time it was quantitated by gravimetric analysis.
Reagents used to precipitate potassium salts include sodium tetraphenylborate, hexachloroplatinic acid, and sodium cobaltinitrite into respectively potassium tetraphenylborate, potassium hexachloroplatinate, and potassium cobaltinitrite. The reaction with sodium cobaltinitrite is illustrative:
- 3 K+
+ Na
3[Co(NO
2)
6] → K
3[Co(NO
2)
6] + 3 Na+
The potassium cobaltinitrite is obtained as a yellow solid.
Commercial uses
Fertilizer

Potassium ions are an essential component of plant nutrition and are found in most soil types. They are used as a fertilizer in agriculture, horticulture, and hydroponic culture in the form of chloride (KCl), sulfate (K
2SO
4), or nitrate (KNO
3), representing the 'K' in 'NPK'. Agricultural fertilizers consume 95% of global potassium chemical production, and about 90% of this potassium is supplied as KCl. The potassium content of most plants ranges from 0.5% to 2% of the harvested weight of crops, conventionally expressed as amount of K
2O. Modern high-yield agriculture depends upon fertilizers to replace the potassium lost at harvest. Most agricultural fertilizers contain potassium chloride, while potassium sulfate is used for chloride-sensitive crops or crops needing higher sulfur content. The sulfate is produced mostly by decomposition of the complex minerals kainite (MgSO
4·KCl·3H2O) and langbeinite (MgSO
4·K
2SO
4). Only a very few fertilizers contain potassium nitrate. In 2005, about 93% of world potassium production was consumed by the fertilizer industry. Furthermore, potassium can play a key role in nutrient cycling by controlling litter composition.
Medical use
Potassium citrate
Potassium citrate is used to treat a kidney stone condition called renal tubular acidosis.
Potassium chloride
Potassium, in the form of potassium chloride is used as a medication to treat and prevent low blood potassium. Low blood potassium may occur due to vomiting, diarrhea, or certain medications. It is given by slow injection into a vein or by mouth.
Food additives
Potassium sodium tartrate (KNaC
4H
4O
6, Rochelle salt) is a main constituent of some varieties of baking powder; it is also used in the silvering of mirrors. Potassium bromate (KBrO
3) is a strong oxidizer (E924), used to improve dough strength and rise height. Potassium bisulfite (KHSO
3) is used as a food preservative, for example in wine and beer-making (but not in meats). It is also used to bleach textiles and straw, and in the tanning of leathers.
Industrial
Major potassium chemicals are potassium hydroxide, potassium carbonate, potassium sulfate, and potassium chloride. Megatons of these compounds are produced annually.
KOH is a strong base, which is used in industry to neutralize strong and weak acids, to control pH and to manufacture potassium salts. It is also used to saponify fats and oils, in industrial cleaners, and in hydrolysis reactions, for example of esters.
Potassium nitrate (KNO
3) or saltpeter is obtained from natural sources such as guano and evaporites or manufactured via the Haber process; it is the oxidant in gunpowder (black powder) and an important agricultural fertilizer. Potassium cyanide (KCN) is used industrially to dissolve copper and precious metals, in particular silver and gold, by forming complexes. Its applications include gold mining, electroplating, and electroforming of these metals; it is also used in organic synthesis to make nitriles. Potassium carbonate (K
2CO
3 or potash) is used in the manufacture of glass, soap, color TV tubes, fluorescent lamps, textile dyes and pigments. Potassium permanganate (KMnO
4) is an oxidizing, bleaching and purification substance and is used for production of saccharin. Potassium chlorate (KClO
3) is added to matches and explosives. Potassium bromide (KBr) was formerly used as a sedative and in photography.
While potassium chromate (K
2CrO
4) is used in the manufacture of a host of different commercial products such as inks, dyes, wood stains (by reacting with the tannic acid in wood), explosives, fireworks, fly paper, and safety matches, as well as in the tanning of leather, all of these uses are due to the chemistry of the chromate ion rather than to that of the potassium ion.
Niche uses
There are thousands of uses of various potassium compounds. One example is potassium superoxide, KO
2, an orange solid that acts as a portable source of oxygen and a carbon dioxide absorber. It is widely used in respiration systems in mines, submarines and spacecraft as it takes less volume than the gaseous oxygen.
- 4 KO
2 + 2 CO
2 → 2 K
2CO
3 + 3 O
2
Another example is potassium cobaltinitrite, K
3[Co(NO
2)
6], which is used as artist's pigment under the name of Aureolin or Cobalt Yellow.
The stable isotopes of potassium can be laser cooled and used to probe fundamental and technological problems in quantum physics. The two bosonic isotopes possess convenient Feshbach resonances to enable studies requiring tunable interactions, while 40
K is one of only two stable fermions amongst the alkali metals.
Laboratory uses
An alloy of sodium and potassium, NaK is a liquid used as a heat-transfer medium and a desiccant for producing dry and air-free solvents. It can also be used in reactive distillation. The ternary alloy of 12% Na, 47% K and 41% Cs has the lowest melting point of −78 °C of any metallic compound.
Metallic potassium is used in several types of magnetometers.
Biological role
Potassium is the eighth or ninth most common element by mass (0.2%) in the human body, so that a 60 kg adult contains a total of about 120 g of potassium. The body has about as much potassium as sulfur and chlorine, and only calcium and phosphorus are more abundant (with the exception of the ubiquitous CHON elements).
Biochemical function
Potassium levels influence multiple physiological processes, including
- resting cellular-membrane potential and the propagation of action potentials in neuronal, muscular, and cardiac tissue. Due to the electrostatic and chemical properties, K+
ions are larger than Na+
ions, and ion channels and pumps in cell membranes can differentiate between the two ions, actively pumping or passively passing one of the two ions while blocking the other. - hormone secretion and action
- vascular tone
- systemic blood pressure control
- gastrointestinal motility
- acid–base homeostasis
- glucose and insulin metabolism
- mineralocorticoid action
- renal concentrating ability
- fluid and electrolyte balance
- local cortical monoaminergic norepinephrine, serotonin, and dopamine levels, and through them, sleep/wake balance, and spontaneous activity.
Homeostasis
Potassium homeostasis denotes the maintenance of the total body potassium content, plasma potassium level, and the ratio of the intracellular to extracellular potassium concentrations within narrow limits, in the face of pulsatile intake (meals), obligatory renal excretion, and shifts between intracellular and extracellular compartments.
Plasma levels
Plasma potassium is normally kept at 3.5 to 5.5 millimoles (mmol) [or milliequivalents (mEq)] per liter by multiple mechanisms. Levels outside this range are associated with an increasing rate of death from multiple causes, and some cardiac, kidney, and lung diseases progress more rapidly if serum potassium levels are not maintained within the normal range.
An average meal of 40–50 mmol presents the body with more potassium than is present in all plasma (20–25 mmol). This surge causes the plasma potassium to rise up to 10% before clearance by renal and extrarenal mechanisms.
Hypokalemia, a deficiency of potassium in the plasma, can be fatal if severe. Common causes are increased gastrointestinal loss (vomiting, diarrhea), and increased renal loss (diuresis). Deficiency symptoms include muscle weakness, paralytic ileus, ECG abnormalities, decreased reflex response; and in severe cases, respiratory paralysis, alkalosis, and cardiac arrhythmia.
Control mechanisms
Potassium content in the plasma is tightly controlled by four basic mechanisms, which have various names and classifications. These are:
- a reactive negative-feedback system,
- a reactive feed-forward system,
- a predictive or circadian system, and
- an internal or cell membrane transport system.
Collectively, the first three are sometimes termed the "external potassium homeostasis system"; and the first two, the "reactive potassium homeostasis system".
- The reactive negative-feedback system refers to the system that induces renal secretion of potassium in response to a rise in the plasma potassium (potassium ingestion, shift out of cells, or intravenous infusion.)
- The reactive feed-forward system refers to an incompletely understood system that induces renal potassium secretion in response to potassium ingestion prior to any rise in the plasma potassium. This is probably initiated by gut cell potassium receptors that detect ingested potassium and trigger vagal afferent signals to the pituitary gland.
- The predictive or circadian system increases renal secretion of potassium during mealtime hours (e.g. daytime for humans, nighttime for rodents) independent of the presence, amount, or absence of potassium ingestion. It is mediated by a circadian oscillator in the suprachiasmatic nucleus of the brain (central clock), which causes the kidney (peripheral clock) to secrete potassium in this rhythmic circadian fashion.

The action of the sodium-potassium pump is an example of primary active transport. The two carrier proteins embedded in the cell membrane on the left are using ATP to move sodium out of the cell against the concentration gradient; The two proteins on the right are using secondary active transport to move potassium into the cell. This process results in reconstitution of ATP. - The ion transport system moves potassium across the cell membrane using two mechanisms. One is active and pumps sodium out of, and potassium into, the cell. The other is passive and allows potassium to leak out of the cell. Potassium and sodium cations influence fluid distribution between intracellular and extracellular compartments by osmotic forces. The movement of potassium and sodium through the cell membrane is mediated by the Na⁺/K⁺-ATPase pump. This ion pump uses ATP to pump three sodium ions out of the cell and two potassium ions into the cell, creating an electrochemical gradient and electromotive force across the cell membrane. The highly selective potassium ion channels (which are tetramers) are crucial for hyperpolarization inside neurons after an action potential is triggered, to cite one example. The most recently discovered potassium ion channel is KirBac3.1, which makes a total of five potassium ion channels (KcsA, KirBac1.1, KirBac3.1, KvAP, and MthK) with a determined structure. All five are from prokaryotic species.
Renal filtration, reabsorption, and excretion
Renal handling of potassium is closely connected to sodium handling. Potassium is the major cation (positive ion) inside animal cells (150 mmol/L, 4.8 g/L), while sodium is the major cation of extracellular fluid (150 mmol/L, 3.345 g/L). In the kidneys, about 180 liters of plasma is filtered through the glomeruli and into the renal tubules per day. This filtering involves about 600 mg of sodium and 33 mg of potassium. Since only 1–10 mg of sodium and 1–4 mg of potassium are likely to be replaced by diet, renal filtering must efficiently reabsorb the remainder from the plasma.
Sodium is reabsorbed to maintain extracellular volume, osmotic pressure, and serum sodium concentration within narrow limits. Potassium is reabsorbed to maintain serum potassium concentration within narrow limits. Sodium pumps in the renal tubules operate to reabsorb sodium. Potassium must be conserved, but because the amount of potassium in the blood plasma is very small and the pool of potassium in the cells is about 30 times as large, the situation is not so critical for potassium. Since potassium is moved passively in counter flow to sodium in response to an apparent (but not actual) Donnan equilibrium, the urine can never sink below the concentration of potassium in serum except sometimes by actively excreting water at the end of the processing. Potassium is excreted twice and reabsorbed three times before the urine reaches the collecting tubules. At that point, urine usually has about the same potassium concentration as plasma. At the end of the processing, potassium is secreted one more time if the serum levels are too high.
With no potassium intake, it is excreted at about 200 mg per day until, in about a week, potassium in the serum declines to a mildly deficient level of 3.0–3.5 mmol/L. If potassium is still withheld, the concentration continues to fall until a severe deficiency causes eventual death.
The potassium moves passively through pores in the cell membrane. When ions move through ion transporters (pumps) there is a gate in the pumps on both sides of the cell membrane and only one gate can be open at once. As a result, approximately 100 ions are forced through per second. Ion channels have only one gate, and there only one kind of ion can stream through, at 10 million to 100 million ions per second. Calcium is required to open the pores, although calcium may work in reverse by blocking at least one of the pores. Carbonyl groups inside the pore on the amino acids mimic the water hydration that takes place in water solution by the nature of the electrostatic charges on four carbonyl groups inside the pore.
Nutrition
Dietary recommendations
The U.S. National Academy of Medicine (NAM), on behalf of both the U.S. and Canada, sets Dietary Reference Intakes, including Estimated Average Requirements (EARs) and Recommended Dietary Allowances (RDAs), or Adequate Intakes (AIs) for when there is not sufficient information to set EARs and RDAs.
For both males and females under 9 years of age, the AIs for potassium are: 400 mg of potassium for 0 to 6-month-old infants, 860 mg of potassium for 7 to 12-month-old infants, 2,000 mg of potassium for 1 to 3-year-old children, and 2,300 mg of potassium for 4 to 8-year-old children.
For males 9 years of age and older, the AIs for potassium are: 2,500 mg of potassium for 9 to 13-year-old males, 3,000 mg of potassium for 14 to 18-year-old males, and 3,400 mg for males that are 19 years of age and older.
For females 9 years of age and older, the AIs for potassium are: 2,300 mg of potassium for 9 to 18-year-old females, and 2,600 mg of potassium for females that are 19 years of age and older.
For pregnant and lactating females, the AIs for potassium are: 2,600 mg of potassium for 14 to 18-year-old pregnant females, 2,900 mg for pregnant females that are 19 years of age and older; furthermore, 2,500 mg of potassium for 14 to 18-year-old lactating females, and 2,800 mg for lactating females that are 19 years of age and older. As for safety, the NAM also sets tolerable upper intake levels (ULs) for vitamins and minerals, but for potassium the evidence was insufficient, so no UL was established.
As of 2004, most Americans adults consume less than 3,000 mg.
Likewise, in the European Union, in particular in Germany, and Italy, insufficient potassium intake is somewhat common. The British National Health Service recommends a similar intake, saying that adults need 3,500 mg per day and that excess amounts may cause health problems such as stomach pain and diarrhea.
In 2019, the National Academies of Sciences, Engineering, and Medicine revised the Adequate Intake for potassium to 2,600 mg/day for females 19 years of age and older who are not pregnant or lactating, and 3,400 mg/day for males 19 years of age and older.
食物摂取源
カリウムはすべての果物、野菜、肉、魚に含まれている。カリウムを多く含む食品としては、ヤム、パセリ、干しアプリコット、牛乳、チョコレートなどがある、 ナッツ類(特にアーモンドとピスタチオ)、ジャガイモ、タケノコ、バナナ、アボカド、ココナッツウォーター、大豆、ふすまなどである。
米国農務省はまた、トマトペースト、オレンジジュース、ビートグリーン、白いんげん豆、プランタン、その他多くのカリウムの食事供給源を、カリウム含有量の多い順にリストアップしている。1日分のカリウムは、プランタン5個分またはバナナ11本分に含まれる。
摂取不足
カリウムの少ない食事は、高血圧や低カリウム血症の原因となる。
サプリメント化
カリウムのサプリメントは、遠位尿細管の上流でナトリウムと水の再吸収を阻害する利尿薬(サイアザイドおよびループ利尿薬)と併用するのが最も広く用いられている。さまざまな処方薬や市販のサプリメントが利用できる。塩化カリウムは水に溶かしてもよいが、塩辛い/苦い味がするため、液体のサプリメントは口に合わない。一般的な用量は10 mmol(400 mg)から20 mmol(800 mg)である。固形錠剤に隣接して発生する非常に高濃度のカリウムイオンは、胃や腸の粘膜を傷つける可能性があるため、カリウムがマトリックスからゆっくりと溶出するように処方されている。このため、米国では非処方のカリウム錠剤は、法律で最大99 mgのカリウムに制限されている。
カリウムの補給は、クエン酸塩や塩化物などの他の代謝産物と組み合わせて、特定の臨床効果を得ることもできる。
カリウムサプリメントは高血圧の影響を緩和し、心血管リスクを軽減するために採用されることがある。塩化カリウムと炭酸水素カリウムは軽度の高血圧をコントロールするのに有用であろう。2020年には、カリウムは米国で33番目に多く処方された医薬品であり、17 万以上の処方があった。カリウムの補給は、本態性高血圧患者の収縮期血圧と拡張期血圧の両方を低下させることが示されている。
さらに、放置すると腎合併症を引き起こす可能性のある腎結石の形成を予防する目的で、カリウムサプリメントが採用されることもある。カリウム濃度が低いと、腎臓でのカルシウム再吸収が低下し、尿中カルシウムの上昇や腎結石の形成リスクが高まる。適切なカリウム濃度を維持することで、このリスクを減らすことができる。
カリウムの作用機序には、細胞膜を横切るカリウムの移動を促進する様々な種類のトランスポーターやチャネルが関与している。このプロセスは、水素イオンの汲み出しを増加させる。その結果、胃酸の分泌が促進され、胃潰瘍の発症につながる可能性がある。
カリウムは骨の健康に関与している。体内の酸塩基平衡に寄与し、骨組織の保護に役立つ。カリウム塩は、骨の健康維持を助けるアルカリ成分を生成する。
糖尿病患者には、特に2型糖尿病患者にはカリウムの補給が必要かもしれない。カリウムは膵臓のβ細胞によるインスリンの分泌に不可欠であり、グルコースレベルを調節するのに役立っている。カリウムが十分でないと、インスリンの分泌が悪くなり、高血糖や糖尿病の悪化につながる。
カリウムの過剰摂取は、胃腸の不快感や心臓のリズムの乱れといった悪影響を及ぼす可能性がある。
カリウムの補給は潰瘍、特に消化性潰瘍疾患に関連して副作用をもたらす可能性がある。カリウムチャネルは胃酸分泌を増加させる可能性があり、潰瘍のリスクを高めることにつながる。消化性潰瘍疾患に使用される医薬品は「プロトンポンプ阻害薬」として知られ、H/K ATPaseを活性化するカリウムポンプを阻害することによって作用する。この阻害作用により、塩酸の胃壁細胞への分泌が抑制され、酸性合成が減少し、潰瘍のリスクが低下する。虚血性心疾患の治療に用いられる薬物であるニコランジルは、硝酸塩およびカリウムATPチャネルを刺激する可能性があり、その結果、消化管潰瘍、口腔潰瘍、肛門潰瘍などの副作用と関連している。カリウムサプリメントの長期的かつ慢性的な使用は、消化管(GI)以外の潰瘍など、より重篤な副作用に関連している。アンジオテンシノーゲン変換酵素阻害薬、アンジオテンシン受容体拮抗薬、カリウム温存利尿薬を服用している患者には、厳重な監視が必要である。
味蕾による検出
カリウムは、濃度に応じて5種類の味覚のうち3種類を誘発するため、味覚で感知することができる。カリウムイオンの希薄溶液は甘味を感じ、牛乳やジュースに適度な濃度で含まれるようになるが、高濃度になると苦味やアルカリ性が増し、最後には塩味も感じるようになる。高濃度カリウム溶液の苦味と塩味の組み合わせは、液体飲料による高用量カリウム補給を嗜好上の難題にしている。
注意事項
| Hazards | |
|---|---|
| GHS labelling: | |
 
| |
| Danger | |
| H260, H314 | |
| P223, P231+P232, P280, P305+P351+P338, P370+P378, P422 | |
| NFPA 704 (fire diamond) | |
金属カリウムは水と激しく反応し、KOHと水素ガスを発生させる。
- 2 K(s) + 2 H
2O(l) → 2 KOH(aq) + H
2(g)↑

この反応は発熱性で、酸素の存在下、生成した水素を発火させるのに十分な熱を放出する。微粉末のカリウムは室温の空気中で発火する。バルクの金属は加熱すると空気中で発火する。密度は0.89 g/cm3であるため、燃焼したカリウムは大気中の酸素にさらされた水に浮く。水を含む多くの一般的な消火剤は効果がないか、カリウム火災を悪化させる。窒素、アルゴン、塩化ナトリウム(食卓塩)、炭酸ナトリウム(ソーダ灰)、二酸化ケイ素(砂)は乾燥していれば有効である。金属火災用のクラスD粉末消火器も有効である。これらの薬剤は火から酸素を奪い、カリウム金属を冷却する。
貯蔵中、カリウムは過酸化物やスーパーオキシドを形成する。これらの過酸化物は油などの有機化合物と激しく反応することがある。過酸化物も過酸化物も金属カリウムと爆発的に反応することがある。
カリウムは空気中の水蒸気と反応するため、通常、無水鉱物油または灯油の下で保管される。リチウムやナトリウムと異なり、カリウムは、不活性(酸素を含まない)雰囲気または真空下でない限り、6ヶ月を超えて油の下で保管すべきではない。空気中で長期間保管すると、衝撃に弱い危険な過酸化物が金属上や容器の蓋の下に形成され、開封時に爆発する恐れがある。
大量のカリウム化合物を摂取すると高カリウム血症を引き起こし、心血管系に強い影響を与える。塩化カリウムはアメリカでは致死注射の処刑に使われる。
こちらも参照
参考文献
- Burkhardt, Elizabeth R. (2006). "Potassium and Potassium Alloys". Ullmann's Encyclopedia of Industrial Chemistry. A22. pp. 31–38. doi:10.1002/14356007.a22_031.pub2. ISBN 978-3-527-30673-2.
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (2007). "Potassium". Lehrbuch der Anorganischen Chemie (in German) (91–100 ed.). Walter de Gruyter. ISBN 978-3-11-017770-1.
- Schultz, H.; Bauer, G.; Schachl, E.; Hagedorn, F.; Schmittinger, P. (2006). "Potassium compounds". Ullmann's Encyclopedia of Industrial Chemistry. A22. pp. 39–103. doi:10.1002/14356007.a22_031.pub2. ISBN 978-3-527-30673-2.
- National Nutrient Database Archived 2014-08-10 at the Wayback Machine at USDA Website
外部リンク
- CID Potassium from PubChem