乳酸カルシウム
Calcium lactate/ja
乳酸カルシウムは、式C
6H
10CaO
6で表される白色の結晶塩で、各カルシウム陽イオンCa2+
に対して2つの乳酸陰イオン H
3C(CHOH)CO−
2からなる。いくつかの水和物を形成するが、最も一般的なものは5水和物C
6H
10CaO
6·5H
2Oである。
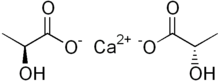
| |
| Names | |
|---|---|
| Preferred IUPAC name
Calcium bis(2-hydroxypropanoate) | |
Other names
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| EC Number |
|
PubChem CID
|
|
| UNII | |
| |
| |
| Properties | |
| C6H10CaO6 | |
| Molar mass | 218.22 g/mol |
| Appearance | white or off-white powder, slightly efflorescent |
| Density | 1.494 g/cm3 |
| Melting point | 240 °C (464 °F; 513 K) (anhydrous) 120 °C (pentahydrate) |
| L-lactate, anhydrous, g/100 mL: 4.8 (10 °C), 5.8 (20 °C), 6.7 (25 °C), 8.5 (30 °C); 7.9 g/100 mL (30 °C) | |
| Solubility | very soluble in methanol, insoluble in ethanol |
| Acidity (pKa) | 6.0-8.5 |
Refractive index (nD)
|
1.470 |
| Pharmacology | |
| A12AA05 (WHO) | |
| Hazards | |
| GHS labelling: | |

| |
| Warning | |
| H319 | |
| P264, P280, P305+P351+P338, P337+P313 | |
| NFPA 704 (fire diamond) | |
| Flash point | Not applicable |
| No data | |
乳酸カルシウムは主にカルシウム欠乏症の治療薬として、またE数がE327の食品添加物として用いられる。 乳酸カルシウムからなるチーズの結晶もある。
特性
乳酸イオンはキラルであり、D(-,R)とL(+,S)の2つのエナンチオマーを持つ。 通常、生物によって合成・代謝されるのはL異性体であるが、一部の細菌はD異性体を生成したり、L異性体をD異性体に変換したりする。
合成プロセスによっては、両者が等量混合したDL塩(ラセミ体)が得られる。 L型もDL型も、熟成したチェダーチーズの表面に結晶として現れる。
L-乳酸カルシウムの水への溶解度は、d-グルコン酸イオンの存在下で著しく増加し、25 °Cで6.7[[::en:gram|g]]/dl)から9.74g/dl以上になる。 逆説的だが、L-乳酸カルシウムの溶解度は10 °C(4.8g/dl)から30 °C(8.5g/dl)まで温度とともに上昇するが、遊離Ca2+
イオンの濃度はほぼ半分に減少する。これは、乳酸イオンとカルシウムイオンが水和しにくくなり、複合体C
3H
5O
3Ca+
を形成するためと説明される。
塩のDL型(ラセミ型)は、純粋なLまたはD異性体よりも水に溶けにくいため、D型を25%でも含む溶液では、L-乳酸塩の代わりにラセミ型のDL-乳酸塩結晶が析出する。
五水和物は35~135℃の乾燥した雰囲気で水分を失い、無水形態に還元されて結晶性を失う。 この過程は25 °C、75%相対湿度で逆転する。
調製法
乳酸カルシウムは、炭酸カルシウムまたは水酸化カルシウムと乳酸の反応によって調製することができる。
19世紀以降、この塩は炭酸カルシウムや水酸化カルシウムなどのカルシウムミネラル源の存在下で炭水化物を発酵させることによって工業的に得られている。発酵は、使用する生物の種類によって、DまたはL乳酸のどちらか、あるいは両方のラセミ混合物を生成する。
用途
医薬
乳酸カルシウムは、ヒトおよび獣医学においていくつかの用途がある。
乳酸カルシウムは制酸剤として医薬品に使われる。
また、低カルシウム血症(カルシウム欠乏症)の治療にも用いられる。さまざまなpHで吸収されるため、食事と一緒に摂取する必要はない。 しかし、この用途ではクエン酸カルシウムよりも利便性が低いことが判明している。乳酸カルシウムは13%の元素状カルシウムを含む。
20世紀初頭、副甲状腺機能不全のヒトや副甲状腺摘出術を受けたイヌのテタニーの予防に、水に溶かした乳酸カルシウムの経口投与が有効であることが判明した(牛乳や錠剤には含まれていない)。
この化合物は、歯石防止剤としてマウスウォッシュや歯磨き粉にも含まれている。
乳酸カルシウム(または他のカルシウム塩)は、可溶性フッ化物の摂取やフッ化水素酸に対する解毒剤である。
食品産業
この化合物は、米国FDAによって一般に安全と認められる(GRAS)として分類される食品添加物であり、固化剤、風味増強剤または着香剤、膨脹剤、栄養補助食品、安定剤および増粘剤として使用される。
乳酸カルシウムは乳を凝固させ、パニールチーズの製造に使われるチェナを作ることから、チーズ乳酸塩としても知られている。 チェナは、さまざまなスイーツや他の乳タンパク質を作るためにも使用される。
乳酸カルシウムは、酸性ピロリン酸ナトリウムを含むいくつかのベーキングパウダーに含まれる成分である。 発酵を遅らせるためにカルシウムを供給する。
乳酸カルシウムは虫歯予防のために無糖食品に添加される。キシリトールを含むチューインガムに添加すると、歯のエナメル質の再石灰化を促進する。
その化合物は、カンタロープなどの切り干し果物にも添加され、彼らの硬さを保ち、保存期間を延長する。これは、同様の目的で使用されるカルシウムクロリドによって引き起こされる苦い味がない。
乳酸カルシウムは分子ガストロノミーにおいて、プレーンおよび逆球形化用の無味脂溶性薬剤として使用される。乳酸カルシウムはアルギン酸ナトリウムと反応して食品の周りに皮を形成する。
動物用飼料
乳酸カルシウムは、カルシウム源として動物の飼料に添加することができる。
化学
この化合物は、以前は食品や医薬品用の乳酸を調製する際の中間体であった。 様々な供給源から得られる不純物の多い酸を乳酸カルシウムに変換し、結晶化によって精製した後、カルシウムを硫酸カルシウムとして沈殿させる硫酸で処理することによって酸に戻した。 この方法では、元の酸を蒸留するよりも純粋な生成物が得られた。 最近では、乳酸アンモニウムがこのプロセスでカルシウムの代わりとして使われるようになった。
水処理
乳酸カルシウムは、塩化アルミニウムAlCl
3に代わる再生可能で無毒、生分解性の凝集剤として、水中の懸濁物質を除去するために考えられてきた。
バイオコンクリート
乳酸カルシウムの添加は、Enterococcus faecalis、Bacillus cohnii、Bacillus pseudofirmus、Sporosarcina pasteuriiなどの細菌がより多くの方解石を生成することを可能にすることによって、バイオコンクリートの圧縮強度を大幅に増加させ、透水性を低下させる。
こちらも参照
