Angiotensin II receptor blocker/ja: Difference between revisions
Created page with "thumb|最初のARBであるロサルタン|250px|right" |
Created page with "===線維症の退縮=== ロサルタンなどのARBは、筋肉、肝臓、心臓、腎臓の線維化を抑制または軽減することが示されている。" |
||
| (36 intermediate revisions by the same user not shown) | |||
| Line 2: | Line 2: | ||
[[Image:Losartan structure.svg|thumb|最初のARBであるロサルタン|250px|right]] | [[Image:Losartan structure.svg|thumb|最初のARBであるロサルタン|250px|right]] | ||
'''アンジオテンシンII受容体拮抗薬'''('''ARBs''')は、正式には'''アンジオテンシンII受容体1型(AT<sub>1</sub>)拮抗薬'''であり、'''アンジオテンシン受容体遮断薬'''、または'''AT<sub>1</sub>受容体拮抗薬'''とも呼ばれる。[[angiotensin II receptor type 1/ja|アンジオテンシンII受容体1型]](AT<sub>1</sub>)に結合して阻害し、それによって[[renin–angiotensin system/ja|レニン・アンジオテンシン系]]の[[Vasoconstriction/ja|動脈管収縮]]および[[sodium retention/ja|ナトリウム貯留]]作用を阻害する一群の医薬品である。 | |||
''' | |||
主な用途は[[hypertension/ja|高血圧]]、[[diabetic nephropathy/ja|糖尿病性腎症]]([[diabetes mellitus/ja|糖尿病]]による[[kidney damage/ja|腎障害]])、[[congestive heart failure/ja|うっ血性心不全]]の治療である。[[ACE inhibitors/ja|ACE阻害薬]]に比べて[[Angiotensin II receptor type 1/ja|AT<sub>1</sub>受容体]]の活性化を''選択的''に[[receptor antagonist/ja|ブロック]]し、[[angiotensin/ja#Angiotensin II|アンジオテンシンII]]の[[Ligand (biochemistry)/ja|結合]]を阻害する。 | |||
ARBと同属のACE阻害薬はともに、[[left ventricular/ja|左心側]][[heart failure/ja|心不全]]の[[hypertension/ja|高血圧]]を発症している患者における第一選択薬の[[antihypertensive/ja|降圧薬]]として適応がある。しかし、ARBはACE阻害薬に比べて副作用が少ないようである。 | |||
==医療用途== | |||
{{Anchor|Medical uses}} | |||
アンジオテンシンII受容体拮抗薬は、主に持続性[[cough/ja|咳嗽]]および/または乾燥性[[cough/ja|咳嗽]]のために[[ACE inhibitor/ja|ACE阻害薬]]治療に耐えられない[[hypertension/ja|高血圧症]]の治療に用いられる。 [[bradykinin/ja|ブラジキニン]]や他の[[kinin/ja|キニン]]の分解を阻害しないため、ACE阻害薬治療を制限するような持続性の空咳および/または[[angioedema/ja|血管浮腫]]を伴うことはまれである。 さらに最近では,ACE阻害薬,特に[[candesartan/ja|カンデサルタン]]療法に不耐容の患者における[[heart failure/ja|心不全]]の治療にも使用されている。[[Irbesartan/ja|イルベサルタン]]と[[losartan/ja|ロサルタン]]は[[type 2 diabetes/ja|2型糖尿病]]の高血圧患者において有益性を示す試験データがあり、[[diabetic nephropathy/ja|糖尿病性腎症]]の進行を遅らせる可能性がある。1998年の二重盲検試験では、[[lisinopril/ja|リシノプリル]]は[[insulin sensitivity/ja|インスリン感受性]]を改善したのに対し、ロサルタンは影響を及ぼさなかった。[[Candesartan/ja|カンデサルタン]]は[[migraine/ja|片頭痛]]の予防的治療に実験的に使用されている。リシノプリルの片頭痛予防効果はカンデサルタンよりも低いことが分かっている。 | |||
アンジオテンシンII受容体拮抗薬には血圧をコントロールするためのさまざまな作用があり、最大投与量における効果は統計的に異なっている。 臨床で使用される場合,必要とされる反応の程度によって使用される薬剤が異なる。 | |||
これらの薬物の中には[[uricosuric/ja|尿毒症]]作用を持つものもある。 | |||
アンジオテンシンIIは、[[AT1 receptor/ja|AT<sub>1</sub>受容体]]刺激を通じて、主要な[[stress hormone/ja|ストレスホルモン]]であり、(ARBは)降圧作用の誘発に加えて、これらの受容体を遮断するため、[[stress-related disorders/ja|ストレス関連障害]]の治療薬として考慮される可能性がある。 | |||
2008年、降圧薬が[[Alzheimer's disease/ja|アルツハイマー病]](AD)と顕著な負の関連を有することが報告された。 米国[[:en:United States Department of Veterans Affairs|退役軍人省]]のシステムで500万人の患者記録をレトロスペクティブに分析したところ、一般的に使用されている降圧医薬品の種類によってADの転帰が大きく異なることがわかった。 アンジオテンシン受容体拮抗薬(ARB)を服用している患者は、他の降圧薬を服用している患者よりもADを発症する可能性が35〜40%低かった。 | |||
1968人の脳卒中患者を対象としたレトロスペクティブ研究で、脳卒中発症前にARBを投与することは、脳卒中の重症度の軽減と転帰の改善をもたらすことが明らかになった。この知見は、ARBが脳保護作用を示すことを示唆する実験データと一致している。 | |||
==副作用== | |||
{{Anchor|Adverse effects}} | |||
このクラスの薬物は通常、忍容性が高い。一般的な[[adverse drug reaction/ja|副作用]](ADR)には、めまい、頭痛、および/または[[hyperkalemia/ja|高カリウム血症]]が含まれる。治療に関連するまれなADRには、初回投与時の[[orthostatic hypotension/ja|起立性低血圧]]、発疹、下痢、[[dyspepsia/ja|消化不良]]、肝機能異常、筋痙攣、[[myalgia/ja|筋肉痛]]、背部痛、[[insomnia/ja|不眠症]]、[[hemoglobin/ja|ヘモグロビン]]値低下、[[renal impairment/ja|腎障害]]、[[pharyngitis/ja|咽頭炎]]、および/または鼻づまりがある。ランダム化比較試験に基づく2014年のコクラン系統的レビューでは、ACE阻害薬を服用している患者とARBを服用している患者を比較した場合、ACE阻害薬を服用している患者に比べてARBを服用している患者では有害事象による試験中止が少なかったと報告されている。 | |||
このクラスの薬剤を使用する主な根拠のひとつは、ACE阻害薬治療に伴う持続的な空咳および/または血管浮腫の回避であるが、それでもまれにこれらが起こることがある。さらに、ACE阻害薬治療で[[angioedema/ja|血管浮腫]]を経験した患者では、交差反応性のリスクもわずかに存在する。 | |||
===心筋梗塞=== | |||
アンジオテンシンII受容体拮抗薬が[[myocardial infarction/ja|心筋梗塞]](MIまたは心臓発作)のリスクをわずかに増加させるかどうかという問題は、現在調査中である。ARBが心筋梗塞のリスクを増加させることを示唆する研究もある。しかし、他の研究ではARBは心筋梗塞のリスクを増加させないとしている。現在までのところ,ARBが心筋梗塞のリスクを増加させる傾向があるかどうかについてのコンセンサスは得られておらず,さらなる研究が進行中である。 | |||
実際、AT<sub>1</sub>遮断の結果として、ARBは[[negative-feedback/ja|負のフィードバック]]ループの結合を解除することにより、アンジオテンシンII濃度をベースラインより数倍上昇させる。循環中のアンジオテンシンII濃度が上昇すると、AT<sub>2</sub>受容体への刺激が阻害されなくなり、その結果、AT<sub>2</sub>受容体の発現も上昇する。しかしながら、最近のデータでは、AT<sub>2</sub>受容体刺激は以前提唱されていたよりも有益ではなく、成長促進、[[fibrosis/ja|線維化]]、[[hypertrophy/ja|肥大]]を媒介し、[[atherogenesis/ja|プロアテローム形成]]や[[proinflammatory/ja|炎症促進]]作用を誘発することにより、特定の状況下では有害でさえある可能性が示唆されている。 | |||
===癌=== | |||
2010年に発表された研究では、ランダム化比較試験のメタアナリシスにより、ARBは新規癌診断のリスクをわずかに増加させることが示唆された。データが限られているため、各薬物に関連するがんの正確なリスクについて結論を出すことはできない。これらの知見はさらなる調査を正当化するものである。 後に米国[[Food and Drug Administration/ja|食品医薬品局]](FDA)が行った、ARBと他の治療法を比較した31のランダム化比較試験のメタアナリシスでは、ARBを投与された患者において、がんの罹患(新規)、がん関連死、乳がん、肺がん、前立腺がんのリスクが上昇したという証拠は認められなかった。2013年、100万人以上の[[:en:veterans|退役軍人]]の経験に関する[[:en:United States Department of Veterans Affairs|米国退役軍人省]]の[[comparative effectiveness research/ja|比較有効性調査]]では、[[lung cancer/ja|肺がん]]または[[prostate cancer/ja|前立腺がん]]のリスク増加は認められなかった。研究者らは次のように結論づけた: "米国退役軍人のこの大規模な全国コホートにおいて、ARBの新規使用者が非使用者に比べて肺癌のリスクが増加するという懸念を支持するエビデンスは認められなかった。我々の所見は、ARBの予防効果と一致していた。" | |||
2013年5月、食品医薬品局の上級規制官であるメディカルチームリーダー、トーマス・A・マーシニアックは、がんリスクの増加はないというFDAの公式結論に反して、入手可能なFDAのデータを患者ごとに検討した結果、ARB患者ではプラセボや他の薬物を服用している患者と比較して肺がんリスクが約24%増加するという結論に達したことを公に明らかにした。マーシニアックが行った批判の一つは、先のFDAのメタアナリシスでは肺[[carcinomas/ja|カルシノーマ]]を癌としてカウントしていないことであった。彼が調査した11の研究のうち10において、ARB群では対照群よりも肺癌症例が多かったとMarciniak氏は述べた。マーシニアクを含む薬物評価部門のチーフであるエリス・アンガーは、この苦情を "陽動"と呼び、インタビューで "われわれは国民に何か新しいことを言う理由はない"と述べたと引用されている。ウォール・ストリート・ジャーナル紙は、この論争に関する記事の中で、他の3人の医師にインタビューし、彼らの意見を聞いている。1人はARBが癌のリスクを増加させることは "間違いない"とし、1人は懸念しており、より多くのデータを見たいとし、3人目は関係がないか、検出が困難で低頻度の関係であると考えている。 | |||
148,334人の患者を含む2016年のメタアナリシスでは、ARBの使用に関連するがん発生率に有意差は認められなかった。 | |||
===腎不全=== | |||
ARBは、[[diabetes/ja|糖尿病]]や[[hypertension/ja|高血圧]]の既往があり、ARBを投与しない患者に対しては腎疾患の発症予防効果があるが、[[proteinuria/ja|蛋白尿]]や[[renal artery stenosis/ja|腎動脈狭窄]]、[[hypertensive nephrosclerosis/ja|高血圧性腎硬化症]]、[[heart failure/ja|心不全]]、[[polycystic kidney disease/ja|多発性嚢胞腎]]、[[chronic kidney disease/ja|慢性腎臓病]]、[[Fibrosis/ja#Heart|間質性線維症]]、[[focal segmental glomerulosclerosis/ja|巣状分節性糸球体硬化症]]、またはARBで治療されているが臨床的にまだ存在する[[hypertension/ja|高血圧症]]などの既往がある患者では、[[serum creatinine/ja|血清クレアチニン]]の上昇に伴う[[glomerular filtration rate/ja|糸球体濾過量]]の減少など、[[kidney function/ja|腎機能]]を悪化させる可能性がある、腎臓への血管の異常な狭窄を引き起こし、臓器への酸素と栄養の供給を遮断するような状態である。 | |||
== 歴史 == | |||
{{Anchor|History}} | |||
{{ | {{main/ja|Discovery and development of angiotensin receptor blockers/ja}} | ||
== 構造 == | |||
{{Anchor|Structure}} | |||
[[Losartan]] | [[Losartan/ja|ロサルタン]]、[[irbesartan/ja|イルベサルタン]]、[[olmesartan/ja|オルメサルタン]]、[[candesartan/ja|カンデサルタン]]、[[valsartan/ja|バルサルタン]]、[[fimasartan/ja|フィマサルタン]]は[[tetrazole/ja|テトラゾール]]基(4つの窒素と1つの炭素を持つ環)を含む。ロサルタン、イルベサルタン、オルメサルタン、カンデサルタン、[[telmisartan/ja|テルミサルタン]]は、1つまたは2つの[[imidazole/ja|イミダゾール]]基を含む。 | ||
==作用機序== | |||
{{Anchor|Mechanism of action}} | |||
これらの物質はAT<sub>1</sub>受容体拮抗薬である;すなわち、[[Angiotensin receptor/ja|アンジオテンシンⅡAT<sub>1</sub>受容体]]の活性化を阻害する。AT<sub>1</sub>受容体は、血管の[[smooth muscle/ja|平滑筋]]細胞、[[adrenal gland/ja|副腎]]の皮質細胞、および[[adrenaline/ja|副腎皮質]]神経シナプスに存在する。AT<sub>1</sub>受容体の遮断は、他の作用の中でも、直接的に[[vasodilation/ja|血管拡張]]を引き起こし、[[vasopressin/ja|バソプレシン]]の分泌を減少させ、[[aldosterone/ja|アルドステロン]]の産生と分泌を減少させる。この複合作用により血圧が低下する。 | |||
このクラスの各ARBの具体的な有効性は、3つの[[pharmacodynamic/ja|薬力学的]](PD)と[[pharmacokinetic/ja|薬物動態学的]](PK)パラメータの組み合わせに依存する。有効性には、有効なレベルでの3つの主要なPD/PK領域が必要である。3つの特性のパラメータを以下のような表にまとめ、重複を排除し、コンセンサス値を得る必要がある。 | |||
===プレッサー阻害=== | |||
[[trough level/ja|トラフレベル]]における[[pressor/ja|プレッサー]]抑制作用。これは、アンジオテンシンIIの血圧上昇(「プレッサー」)作用の遮断または阻害の程度に関係する。 しかし、プレッサー抑制は血圧降下(BP)効果の''それ自体''の指標ではない。 米国[[Food and Drug Administration/ja|食品医薬品局]](FDA)の添付文書(PI)に記載されているARBの24時間目におけるこの作用の抑制率は以下の通りである: | |||
[[ | * [[Valsartan/ja|バルサルタン]]{{snd}}80 mgで30% | ||
* [[Valsartan]]{{snd}} | * [[Telmisartan/ja|テルミサルタン]]{{snd}}80 mgで40% | ||
* [[Telmisartan]]{{snd}} | * [[Losartan/ja|ロサルタン]]{{snd}} 100 mgで25~40%。100 mgで25-40% | ||
* [[Losartan]]{{snd}} | * [[Irbesartan/ja|イルベサルタン]]{{snd}}150 mgで40%; 300 mgで60 | ||
* [[Irbesartan]]{{snd}} | * [[Azilsartan/ja|アジルサルタン]]{{snd}}32 mgで60% | ||
* [[Azilsartan]]{{snd}} | * [[Olmesartan/ja|オルメサルタン]]{{snd}}20 mgで61%; 40 mgで74% | ||
* [[Olmesartan]]{{snd}} | |||
===AT<sub>1</sub>親和性 vs AT<sub>2</sub>親和性=== | |||
===AT<sub>1</sub> | |||
特定のARBの結合親和性におけるAT<sub>1</sub>とAT<sub>2</sub>の比を以下に示す。しかし、AT<sub>1</sub>親和性対AT<sub>2</sub>親和性は血圧反応の指標としては意味がない。 | |||
* [[Losartan/ja|ロサルタン]]{{snd}} 1000倍 | |||
* [[Losartan]]{{snd}} | * [[Telmisartan/ja|テルミサルタン]]{{snd}} 3000倍 | ||
* [[Telmisartan]]{{snd}} | * [[Irbesartan/ja|イルベサルタン]]{{snd}} 8500倍 | ||
* [[Irbesartan]]{{snd}} | * [[Candesartan/ja|カンデサルタン]]{{snd}} 10000倍以上 | ||
* [[Candesartan]]{{snd}} | * [[Olmesartan/ja|オルメサルタン]]{{snd}} 12500倍 | ||
* [[Olmesartan]]{{snd}} | * [[Valsartan/ja|バルサルタン]]{{snd}} 30000倍 | ||
* [[Valsartan]]{{snd}} | * [[Saprisartan/ja|サプリサルタン]] – ??? | ||
* [[Saprisartan]] – ??? | |||
===構成要素=== | |||
=== | |||
[[telmisartan/ja|テルミサルタン]]と[[eprosartan/ja|エプロサルタン]]を除くほぼすべてのARBは[[biphenyltetrazole moiety/ja|ビフェニルテトラゾール部位]]を含む。 | |||
===有効成分=== | |||
=== | |||
ロサルタンは[[heterocycle imidazole/ja|複素環イミダゾール]]を持つが、バルサルタンは非平面アシル化[[amino acid/ja|アミノ酸]]を持つ。 | |||
==薬物動態の比較== | |||
{{Anchor|Pharmacokinetics comparison}} | |||
{| class="wikitable" | {| class="wikitable" | ||
|+ | |+ 表1: ARB[[pharmacokinetics/ja|薬物動態]]の比較 | ||
|- | |- | ||
! | ! 薬剤 | ||
! | ! 製品名 | ||
! [[Biological half-life]] [ | ! [[Biological half-life/ja|半減期]] [時間] | ||
! [[Cmax_(pharmacology)| | ! [[Cmax_(pharmacology)/ja|ピーク血漿中濃度[Tmax]]] | ||
! [[Protein binding]] [%] | ! [[Protein binding/ja|タンパク質結合率]] [%] | ||
! [[Bioavailability]] [%] | ! [[Bioavailability/ja|生物学的利用能]] [%] | ||
! | ! 腎/肝[[Clearance (medicine)/ja|クリアランス]] [%] | ||
! | ! 食べ物の影響 | ||
! | ! 容量/日 [mg] | ||
! [[Metabolism]]/[[Transport protein| | ! [[Metabolism/ja|代謝]]/[[Transport protein/ja|トランスポーター]] | ||
|- | |- | ||
| [[Losartan]] | | [[Losartan/ja|ロサルタン]] | ||
| Cozaar | | Cozaar | ||
| | | 2H | ||
| | | 1H | ||
| 98.7% | | 98.7% | ||
| 33% | | 33% | ||
| 10/90% | | 10/90% | ||
| | | ミネラル | ||
| 50–100 | | 50–100 | ||
| [[Sensitive substrates]]: [[CYP2C9]] | | [[Sensitive substrates/ja|センシティブ基質]]: [[CYP2C9/ja|CYP2C9]]と[[CYP3A4/ja|CYP3A4]] | ||
|- | |- | ||
| [[Losartan#Pharmacokinetics|EXP 3174]] | | [[Losartan/ja#Pharmacokinetics|EXP 3174]] ロサルタンの活性代謝物 | ||
| - | | - | ||
| | | 6–9H | ||
| | | ロサルタン経口投与3–4H後 | ||
| 99.8% | | 99.8% | ||
| – | | – | ||
| Line 175: | Line 122: | ||
| – | | – | ||
| – | | – | ||
| | | AUCはフェニトインで63%、リファンピンで40%減少する;特定のCYP450アイソザイムは不明 | ||
|- | |- | ||
| [[Candesartan]] | | [[Candesartan/ja|カンデサルタン]] | ||
| Atacand | | Atacand | ||
| 9 | | 9 | ||
| | | 3–4H | ||
| >99% | | >99% | ||
| 15% | | 15% | ||
| Line 186: | Line 133: | ||
| No | | No | ||
| 4–32 | | 4–32 | ||
| [[Moderate sensitive substrate/ja|中程度のセンシティブ基質]]: [[CYP2C9/ja|CYP2C9]] | |||
| [[Moderate sensitive substrate]]: [[CYP2C9]] | |||
|- | |- | ||
| [[Valsartan]] | | [[Valsartan/ja|バルサルタン]] | ||
| Diovan | | Diovan | ||
| 6 | | 6 | ||
| | | 2–4H | ||
| 95% | | 95% | ||
| 25% | | 25% | ||
| Line 203: | Line 146: | ||
| Yes | | Yes | ||
| 80–320 | | 80–320 | ||
| | | 基質: [[Multidrug resistance-associated protein 2/ja|MRP2]]と[[OATP1B1/ja|OATP1B1/SLCO1B1]] | ||
|- | |- | ||
| [[Irbesartan]] | | [[Irbesartan/ja|イルベサルタン]] | ||
| Avapro | | Avapro | ||
| 11–15 | | 11–15 | ||
| 1. | | 1.5–2H | ||
| 90–95% | | 90–95% | ||
| 70% | | 70% | ||
| Line 214: | Line 157: | ||
| No | | No | ||
| 150–300 | | 150–300 | ||
| | | [[CYP2C9/ja|CYP2C9]]のマイナー基質 | ||
|- | |- | ||
| [[Telmisartan]] | | [[Telmisartan/ja|テルミサルタン]] | ||
| Micardis | | Micardis | ||
| 24 | | 24 | ||
| 0. | | 0.5–1H | ||
| >99% | | >99% | ||
| 42–58% | | 42–58% | ||
| Line 225: | Line 168: | ||
| No | | No | ||
| 40–80 | | 40–80 | ||
| | | 不明; >97% 胆汁排泄 | ||
|- | |- | ||
| [[Eprosartan]] | | [[Eprosartan/ja|エプロサルタン]] | ||
| Teveten | | Teveten | ||
| 5 | | 5 | ||
| | | 1–2H | ||
| 98% | | 98% | ||
| 13% | | 13% | ||
| Line 236: | Line 179: | ||
| No | | No | ||
| 400–800 | | 400–800 | ||
| | | 不明; >90% 腎と胆汁排泄 | ||
|- | |- | ||
| [[Olmesartan]] | | [[Olmesartan/ja|オルメサルタン]] | ||
| Benicar/Olmetec | | Benicar/Olmetec | ||
| 14–16 | | 14–16 | ||
| | | 1–2H | ||
| >99% | | >99% | ||
| 29% | | 29% | ||
| Line 247: | Line 190: | ||
| No | | No | ||
| 10–40 | | 10–40 | ||
| | | [[OATP1B1/ja|OATP1B1/SLCO1B1]]の基質 | ||
|- | |- | ||
| [[Azilsartan]] | | [[Azilsartan/jaZ|アジルサルタン]] | ||
| Edarbi | | Edarbi | ||
| 11 | | 11 | ||
| 1. | | 1.5–3H | ||
| >99% | | >99% | ||
| 60% | | 60% | ||
| Line 258: | Line 201: | ||
| No | | No | ||
| 40–80 | | 40–80 | ||
| | | CYP2C9のマイナー基質 | ||
|- | |- | ||
| [[Fimasartan]] | | [[Fimasartan/ja|フィマサルタン]] | ||
| Kanarb | | Kanarb | ||
| 7–11 | | 7–11 | ||
| | | 服用後0.5–3H | ||
| >97% | | >97% | ||
| 30–40% | | 30–40% | ||
| Line 269: | Line 212: | ||
| – | | – | ||
| 30–120 | | 30–120 | ||
| | | 不明; 主に胆汁性排泄 | ||
|- | |- | ||
! | ! 薬剤 | ||
! | ! 製品名 | ||
! [[Biological half-life]] [ | ! [[Biological half-life/ja|半減期]] [時間] | ||
! [[Cmax_(pharmacology)| | ! [[Cmax_(pharmacology)/ja|ピーク血漿中濃度[Tmax]]] | ||
! [[Protein binding]] [%] | ! [[Protein binding/ja|タンパク質結合率]] [%] | ||
! [[Bioavailability]] [%] | ! [[Bioavailability/ja|生物学的利用能]] [%] | ||
! | ! 腎/肝[[Clearance (medicine)/ja|クリアランス]] [%] | ||
! | ! 食べ物の影響 | ||
! | ! 容量/日 [mg] | ||
! [[Metabolism]]/[[Transport protein| | ! [[Metabolism/ja|代謝]]/[[Transport protein/ja|トランスポーター]] | ||
|} | |} | ||
{{further/ja|Discovery and development of angiotensin receptor blockers/ja}} | |||
{{further|Discovery and development of angiotensin receptor blockers}} | |||
==研究== | |||
{{Anchor|Research}} | |||
=== | ===寿命=== | ||
AT<sub>1</sub>をコードするAgtr1a遺伝子をノックアウトすると、マウスの寿命は対照と比較して26%著しく延長する。 そのメカニズムとしては、酸化的損傷(特にミトコンドリア)の軽減と腎臓の生存促進遺伝子の過剰発現が考えられる。ARBにも同様の効果があるようだ。 | |||
===線維症の退縮=== | |||
=== | ロサルタンなどのARBは、筋肉、肝臓、心臓、腎臓の線維化を抑制または軽減することが示されている。 | ||
===大動脈基部拡張の退縮=== | |||
== | カンデサルタンとバルサルタンを用いた2003年の研究では、拡張した[[Ascending aorta/ja|大動脈起始部]]のサイズを退縮させる能力が示された。 | ||
==不純物== | |||
{{Anchor|Impurities}} | |||
{{Anchor|recalls}} | {{Anchor|recalls}} | ||
{{See also|Ranitidine#impurities}} | {{See also/ja|Ranitidine/ja#impurities}} | ||
=== | ===ニトロソアミン=== | ||
2018年と2019年、米国[[Food and Drug Administration/ja|食品医薬品局]](FDA)は、アンジオテンシンII受容体拮抗薬(ARB)製剤[[valsartan/ja|バルサルタン]]、[[losartan/ja|ロサルタン]]、[[irbesartan/ja|イルベサルタン]]にNDMAとNDEAの不純物の痕跡を発見した。FDAは"2018年6月、FDAはある[[active ingredient/ja|API]]生産者から[[N-Nitrosodimethylamine/ja|N-ニトロソジメチルアミン]](NDMA)と特定される不純物の存在を知らされた。それ以来、FDAは、他のタイプの[[nitrosamine/ja|ニトロソアミン]]化合物、例えば[[N-Nitrosodiethylamine/ja|N-ニトロソジエチルアミン]](NDEA)が、バルサルタンおよびARBクラスの他の薬物の複数のAPI生産者のAPI中に許容できないレベルで存在すると判断した。" 2018年、FDAは業界に対し、不純物の評価と管理方法に関するガイダンスを発表した。 | |||
2020年8月、[[:en:European Medicines Agency|欧州医薬品庁]](EMA)は、ヒト用医薬品中のニトロソアミン不純物の存在を回避する方法について製造販売承認者にガイダンスを提供し、ニトロソアミンの存在の可能性についてすべての化学・生物学的ヒト用医薬品をレビューし、リスクのある製品をテストするよう求めた。 | |||
2020年11月、EMAの[[:en:Committee for Medicinal Products for Human Use|医薬品委員会]](CHMP)は、サルタン医薬品のニトロソアミン不純物の制限に関する勧告を、他のクラスの医薬品に対して出した勧告と整合させた。主な変更点はニトロソアミンの規制値に関するもので、これまでは有効成分に適用されていたが、最終製品(錠剤など)に適用されるようになった。この規制値は国際的に合意された基準(ICH M7(R1))に基づくもので、サルタン製剤に含まれるニトロソアミンによる癌の過剰リスクが、生涯治療のために服用する人の場合、10万分の1以下であることを保証しなければならない。 | |||
これらのサルタン製剤は特定の環構造(テトラゾール)を有しており、その合成によりニトロソアミン不純物が生成される可能性がある。アジルサルタン、エプロサルタン、テルミサルタンなど、このような環を持たない他のサルタン製剤は、今回のレビューには含まれていないが、後続の他の医薬品のレビューでカバーされている。 | |||
===アジド化合物=== | |||
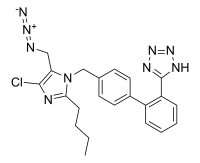
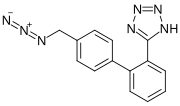
== | {{multiple image | width1 = 200 | image1 = Losartan azide.svg | alt1 = ロサルタンアジドの骨格式 | width2 = 180 | image2 = AZBT.svg | alt2 = アジドメチル-ビフェニル-テトラゾールの骨格式 | footer = ロサルタンアジド(左)とAZBT(右)、サルタンから検出される2つのアジドプロセス不純物。ロサルタンアジドはロサルタンの製造時にのみ発生し、AZBTは同クラスの複数の薬物に含まれる。}} | ||
{{multiple image | width1 = 200 | image1 = Losartan azide.svg | alt1 = | 2021年4月、[[:en:European Directorate for the Quality of Medicines & HealthCare|欧州医薬品品質理事会]](EDQM)は、テトラゾール含有サルタンに非ニトロソアミン系不純物(具体的には[[azide/ja|アジド化合物]])が混入するリスクがあることを警告した。2021年9月、EDQMは調査によりロサルタンのみに存在する新規のアジド系不純物(ロサルタンアジドまたはロサルタンアジド不純物)が発見され、[[Ames test/ja|エームス試験]]で変異原性が認められたと発表した。 | ||
その後、2021年と2022年にロサルタン、イルベサルタン、バルサルタンにアジド系不純物の混入が数例検出され、[[:en:Australia|オーストラリア]]、[[:en:Brazil|ブラジル]]、欧州(スイスを含む)で調査から市場撤去、予防的回収に至る規制当局の対応が行われた。 | |||
[[Teva Pharmaceuticals]]は、これらの不純物の混入を防ぐためにロサルタンの製造工程を変更すると発表し、インドの原薬メーカーであるIOLケミカルズ・アンド・ファーマシューティカルズは、アジド汚染物質を含まないように設計されたロサルタンの新しい合成に関する特許を申請した。 | |||
[[Teva Pharmaceuticals]] | |||
{{clear}} | {{clear}} | ||
== 外部リンク == | |||
* {{MeshName|Angiotensin II Type 1 Receptor Blockers}} | * {{MeshName|Angiotensin II Type 1 Receptor Blockers}} | ||
* {{cite web | title=Nitrosamine impurities in medications: Guidance | website=Health Canada | date=4 April 2022 | url=https://www.canada.ca/en/health-canada/services/drugs-health-products/compliance-enforcement/information-health-product/drugs/nitrosamine-impurities/medications-guidance.html }} | * {{cite web | title=Nitrosamine impurities in medications: Guidance | website=Health Canada | date=4 April 2022 | url=https://www.canada.ca/en/health-canada/services/drugs-health-products/compliance-enforcement/information-health-product/drugs/nitrosamine-impurities/medications-guidance.html }} | ||
{{Major drug groups/ja}} | |||
{{Major drug groups}} | {{Receptor agonists and antagonists/ja}} | ||
{{Receptor agonists and antagonists}} | {{Angiotensin II receptor antagonists/ja}} | ||
{{Angiotensin II receptor antagonists}} | {{Angiotensin receptor modulators/ja}} | ||
{{Angiotensin receptor modulators}} | |||
{{Portal bar | Medicine}} | {{Portal bar | Medicine}} | ||
{{DEFAULTSORT:Angiotensin Ii Receptor Blocker}} | {{DEFAULTSORT:Angiotensin Ii Receptor Blocker}} | ||
[[Category:Angiotensin II receptor antagonists| ]] | [[Category:Angiotensin II receptor antagonists| ]] | ||
Latest revision as of 08:58, 27 March 2024
アンジオテンシンII受容体拮抗薬(ARBs)は、正式にはアンジオテンシンII受容体1型(AT1)拮抗薬であり、アンジオテンシン受容体遮断薬、またはAT1受容体拮抗薬とも呼ばれる。アンジオテンシンII受容体1型(AT1)に結合して阻害し、それによってレニン・アンジオテンシン系の動脈管収縮およびナトリウム貯留作用を阻害する一群の医薬品である。
主な用途は高血圧、糖尿病性腎症(糖尿病による腎障害)、うっ血性心不全の治療である。ACE阻害薬に比べてAT1受容体の活性化を選択的にブロックし、アンジオテンシンIIの結合を阻害する。
ARBと同属のACE阻害薬はともに、左心側心不全の高血圧を発症している患者における第一選択薬の降圧薬として適応がある。しかし、ARBはACE阻害薬に比べて副作用が少ないようである。
医療用途
アンジオテンシンII受容体拮抗薬は、主に持続性咳嗽および/または乾燥性咳嗽のためにACE阻害薬治療に耐えられない高血圧症の治療に用いられる。 ブラジキニンや他のキニンの分解を阻害しないため、ACE阻害薬治療を制限するような持続性の空咳および/または血管浮腫を伴うことはまれである。 さらに最近では,ACE阻害薬,特にカンデサルタン療法に不耐容の患者における心不全の治療にも使用されている。イルベサルタンとロサルタンは2型糖尿病の高血圧患者において有益性を示す試験データがあり、糖尿病性腎症の進行を遅らせる可能性がある。1998年の二重盲検試験では、リシノプリルはインスリン感受性を改善したのに対し、ロサルタンは影響を及ぼさなかった。カンデサルタンは片頭痛の予防的治療に実験的に使用されている。リシノプリルの片頭痛予防効果はカンデサルタンよりも低いことが分かっている。
アンジオテンシンII受容体拮抗薬には血圧をコントロールするためのさまざまな作用があり、最大投与量における効果は統計的に異なっている。 臨床で使用される場合,必要とされる反応の程度によって使用される薬剤が異なる。
これらの薬物の中には尿毒症作用を持つものもある。
アンジオテンシンIIは、AT1受容体刺激を通じて、主要なストレスホルモンであり、(ARBは)降圧作用の誘発に加えて、これらの受容体を遮断するため、ストレス関連障害の治療薬として考慮される可能性がある。
2008年、降圧薬がアルツハイマー病(AD)と顕著な負の関連を有することが報告された。 米国退役軍人省のシステムで500万人の患者記録をレトロスペクティブに分析したところ、一般的に使用されている降圧医薬品の種類によってADの転帰が大きく異なることがわかった。 アンジオテンシン受容体拮抗薬(ARB)を服用している患者は、他の降圧薬を服用している患者よりもADを発症する可能性が35〜40%低かった。
1968人の脳卒中患者を対象としたレトロスペクティブ研究で、脳卒中発症前にARBを投与することは、脳卒中の重症度の軽減と転帰の改善をもたらすことが明らかになった。この知見は、ARBが脳保護作用を示すことを示唆する実験データと一致している。
副作用
このクラスの薬物は通常、忍容性が高い。一般的な副作用(ADR)には、めまい、頭痛、および/または高カリウム血症が含まれる。治療に関連するまれなADRには、初回投与時の起立性低血圧、発疹、下痢、消化不良、肝機能異常、筋痙攣、筋肉痛、背部痛、不眠症、ヘモグロビン値低下、腎障害、咽頭炎、および/または鼻づまりがある。ランダム化比較試験に基づく2014年のコクラン系統的レビューでは、ACE阻害薬を服用している患者とARBを服用している患者を比較した場合、ACE阻害薬を服用している患者に比べてARBを服用している患者では有害事象による試験中止が少なかったと報告されている。
このクラスの薬剤を使用する主な根拠のひとつは、ACE阻害薬治療に伴う持続的な空咳および/または血管浮腫の回避であるが、それでもまれにこれらが起こることがある。さらに、ACE阻害薬治療で血管浮腫を経験した患者では、交差反応性のリスクもわずかに存在する。
心筋梗塞
アンジオテンシンII受容体拮抗薬が心筋梗塞(MIまたは心臓発作)のリスクをわずかに増加させるかどうかという問題は、現在調査中である。ARBが心筋梗塞のリスクを増加させることを示唆する研究もある。しかし、他の研究ではARBは心筋梗塞のリスクを増加させないとしている。現在までのところ,ARBが心筋梗塞のリスクを増加させる傾向があるかどうかについてのコンセンサスは得られておらず,さらなる研究が進行中である。
実際、AT1遮断の結果として、ARBは負のフィードバックループの結合を解除することにより、アンジオテンシンII濃度をベースラインより数倍上昇させる。循環中のアンジオテンシンII濃度が上昇すると、AT2受容体への刺激が阻害されなくなり、その結果、AT2受容体の発現も上昇する。しかしながら、最近のデータでは、AT2受容体刺激は以前提唱されていたよりも有益ではなく、成長促進、線維化、肥大を媒介し、プロアテローム形成や炎症促進作用を誘発することにより、特定の状況下では有害でさえある可能性が示唆されている。
癌
2010年に発表された研究では、ランダム化比較試験のメタアナリシスにより、ARBは新規癌診断のリスクをわずかに増加させることが示唆された。データが限られているため、各薬物に関連するがんの正確なリスクについて結論を出すことはできない。これらの知見はさらなる調査を正当化するものである。 後に米国食品医薬品局(FDA)が行った、ARBと他の治療法を比較した31のランダム化比較試験のメタアナリシスでは、ARBを投与された患者において、がんの罹患(新規)、がん関連死、乳がん、肺がん、前立腺がんのリスクが上昇したという証拠は認められなかった。2013年、100万人以上の退役軍人の経験に関する米国退役軍人省の比較有効性調査では、肺がんまたは前立腺がんのリスク増加は認められなかった。研究者らは次のように結論づけた: "米国退役軍人のこの大規模な全国コホートにおいて、ARBの新規使用者が非使用者に比べて肺癌のリスクが増加するという懸念を支持するエビデンスは認められなかった。我々の所見は、ARBの予防効果と一致していた。"
2013年5月、食品医薬品局の上級規制官であるメディカルチームリーダー、トーマス・A・マーシニアックは、がんリスクの増加はないというFDAの公式結論に反して、入手可能なFDAのデータを患者ごとに検討した結果、ARB患者ではプラセボや他の薬物を服用している患者と比較して肺がんリスクが約24%増加するという結論に達したことを公に明らかにした。マーシニアックが行った批判の一つは、先のFDAのメタアナリシスでは肺カルシノーマを癌としてカウントしていないことであった。彼が調査した11の研究のうち10において、ARB群では対照群よりも肺癌症例が多かったとMarciniak氏は述べた。マーシニアクを含む薬物評価部門のチーフであるエリス・アンガーは、この苦情を "陽動"と呼び、インタビューで "われわれは国民に何か新しいことを言う理由はない"と述べたと引用されている。ウォール・ストリート・ジャーナル紙は、この論争に関する記事の中で、他の3人の医師にインタビューし、彼らの意見を聞いている。1人はARBが癌のリスクを増加させることは "間違いない"とし、1人は懸念しており、より多くのデータを見たいとし、3人目は関係がないか、検出が困難で低頻度の関係であると考えている。
148,334人の患者を含む2016年のメタアナリシスでは、ARBの使用に関連するがん発生率に有意差は認められなかった。
腎不全
ARBは、糖尿病や高血圧の既往があり、ARBを投与しない患者に対しては腎疾患の発症予防効果があるが、蛋白尿や腎動脈狭窄、高血圧性腎硬化症、心不全、多発性嚢胞腎、慢性腎臓病、間質性線維症、巣状分節性糸球体硬化症、またはARBで治療されているが臨床的にまだ存在する高血圧症などの既往がある患者では、血清クレアチニンの上昇に伴う糸球体濾過量の減少など、腎機能を悪化させる可能性がある、腎臓への血管の異常な狭窄を引き起こし、臓器への酸素と栄養の供給を遮断するような状態である。
歴史
構造
ロサルタン、イルベサルタン、オルメサルタン、カンデサルタン、バルサルタン、フィマサルタンはテトラゾール基(4つの窒素と1つの炭素を持つ環)を含む。ロサルタン、イルベサルタン、オルメサルタン、カンデサルタン、テルミサルタンは、1つまたは2つのイミダゾール基を含む。
作用機序
これらの物質はAT1受容体拮抗薬である;すなわち、アンジオテンシンⅡAT1受容体の活性化を阻害する。AT1受容体は、血管の平滑筋細胞、副腎の皮質細胞、および副腎皮質神経シナプスに存在する。AT1受容体の遮断は、他の作用の中でも、直接的に血管拡張を引き起こし、バソプレシンの分泌を減少させ、アルドステロンの産生と分泌を減少させる。この複合作用により血圧が低下する。
このクラスの各ARBの具体的な有効性は、3つの薬力学的(PD)と薬物動態学的(PK)パラメータの組み合わせに依存する。有効性には、有効なレベルでの3つの主要なPD/PK領域が必要である。3つの特性のパラメータを以下のような表にまとめ、重複を排除し、コンセンサス値を得る必要がある。
プレッサー阻害
トラフレベルにおけるプレッサー抑制作用。これは、アンジオテンシンIIの血圧上昇(「プレッサー」)作用の遮断または阻害の程度に関係する。 しかし、プレッサー抑制は血圧降下(BP)効果のそれ自体の指標ではない。 米国食品医薬品局(FDA)の添付文書(PI)に記載されているARBの24時間目におけるこの作用の抑制率は以下の通りである:
- バルサルタン – 80 mgで30%
- テルミサルタン – 80 mgで40%
- ロサルタン – 100 mgで25~40%。100 mgで25-40%
- イルベサルタン – 150 mgで40%; 300 mgで60
- アジルサルタン – 32 mgで60%
- オルメサルタン – 20 mgで61%; 40 mgで74%
AT1親和性 vs AT2親和性
特定のARBの結合親和性におけるAT1とAT2の比を以下に示す。しかし、AT1親和性対AT2親和性は血圧反応の指標としては意味がない。
- ロサルタン – 1000倍
- テルミサルタン – 3000倍
- イルベサルタン – 8500倍
- カンデサルタン – 10000倍以上
- オルメサルタン – 12500倍
- バルサルタン – 30000倍
- サプリサルタン – ???
構成要素
テルミサルタンとエプロサルタンを除くほぼすべてのARBはビフェニルテトラゾール部位を含む。
有効成分
ロサルタンは複素環イミダゾールを持つが、バルサルタンは非平面アシル化アミノ酸を持つ。
薬物動態の比較
| 薬剤 | 製品名 | 半減期 [時間] | ピーク血漿中濃度[Tmax] | タンパク質結合率 [%] | 生物学的利用能 [%] | 腎/肝クリアランス [%] | 食べ物の影響 | 容量/日 [mg] | 代謝/トランスポーター |
|---|---|---|---|---|---|---|---|---|---|
| ロサルタン | Cozaar | 2H | 1H | 98.7% | 33% | 10/90% | ミネラル | 50–100 | センシティブ基質: CYP2C9とCYP3A4 |
| EXP 3174 ロサルタンの活性代謝物 | - | 6–9H | ロサルタン経口投与3–4H後 | 99.8% | – | 50/50% | – | – | AUCはフェニトインで63%、リファンピンで40%減少する;特定のCYP450アイソザイムは不明 |
| カンデサルタン | Atacand | 9 | 3–4H | >99% | 15% | 60/40% | No | 4–32 | 中程度のセンシティブ基質: CYP2C9 |
| バルサルタン | Diovan | 6 | 2–4H | 95% | 25% | 30/70% | Yes | 80–320 | 基質: MRP2とOATP1B1/SLCO1B1 |
| イルベサルタン | Avapro | 11–15 | 1.5–2H | 90–95% | 70% | 20/80% | No | 150–300 | CYP2C9のマイナー基質 |
| テルミサルタン | Micardis | 24 | 0.5–1H | >99% | 42–58% | 1/99% | No | 40–80 | 不明; >97% 胆汁排泄 |
| エプロサルタン | Teveten | 5 | 1–2H | 98% | 13% | 30/70% | No | 400–800 | 不明; >90% 腎と胆汁排泄 |
| オルメサルタン | Benicar/Olmetec | 14–16 | 1–2H | >99% | 29% | 40/60% | No | 10–40 | OATP1B1/SLCO1B1の基質 |
| アジルサルタン | Edarbi | 11 | 1.5–3H | >99% | 60% | 55/42% | No | 40–80 | CYP2C9のマイナー基質 |
| フィマサルタン | Kanarb | 7–11 | 服用後0.5–3H | >97% | 30–40% | – | – | 30–120 | 不明; 主に胆汁性排泄 |
| 薬剤 | 製品名 | 半減期 [時間] | ピーク血漿中濃度[Tmax] | タンパク質結合率 [%] | 生物学的利用能 [%] | 腎/肝クリアランス [%] | 食べ物の影響 | 容量/日 [mg] | 代謝/トランスポーター |
研究
寿命
AT1をコードするAgtr1a遺伝子をノックアウトすると、マウスの寿命は対照と比較して26%著しく延長する。 そのメカニズムとしては、酸化的損傷(特にミトコンドリア)の軽減と腎臓の生存促進遺伝子の過剰発現が考えられる。ARBにも同様の効果があるようだ。
線維症の退縮
ロサルタンなどのARBは、筋肉、肝臓、心臓、腎臓の線維化を抑制または軽減することが示されている。
大動脈基部拡張の退縮
カンデサルタンとバルサルタンを用いた2003年の研究では、拡張した大動脈起始部のサイズを退縮させる能力が示された。
不純物
ニトロソアミン
2018年と2019年、米国食品医薬品局(FDA)は、アンジオテンシンII受容体拮抗薬(ARB)製剤バルサルタン、ロサルタン、イルベサルタンにNDMAとNDEAの不純物の痕跡を発見した。FDAは"2018年6月、FDAはあるAPI生産者からN-ニトロソジメチルアミン(NDMA)と特定される不純物の存在を知らされた。それ以来、FDAは、他のタイプのニトロソアミン化合物、例えばN-ニトロソジエチルアミン(NDEA)が、バルサルタンおよびARBクラスの他の薬物の複数のAPI生産者のAPI中に許容できないレベルで存在すると判断した。" 2018年、FDAは業界に対し、不純物の評価と管理方法に関するガイダンスを発表した。
2020年8月、欧州医薬品庁(EMA)は、ヒト用医薬品中のニトロソアミン不純物の存在を回避する方法について製造販売承認者にガイダンスを提供し、ニトロソアミンの存在の可能性についてすべての化学・生物学的ヒト用医薬品をレビューし、リスクのある製品をテストするよう求めた。
2020年11月、EMAの医薬品委員会(CHMP)は、サルタン医薬品のニトロソアミン不純物の制限に関する勧告を、他のクラスの医薬品に対して出した勧告と整合させた。主な変更点はニトロソアミンの規制値に関するもので、これまでは有効成分に適用されていたが、最終製品(錠剤など)に適用されるようになった。この規制値は国際的に合意された基準(ICH M7(R1))に基づくもので、サルタン製剤に含まれるニトロソアミンによる癌の過剰リスクが、生涯治療のために服用する人の場合、10万分の1以下であることを保証しなければならない。
これらのサルタン製剤は特定の環構造(テトラゾール)を有しており、その合成によりニトロソアミン不純物が生成される可能性がある。アジルサルタン、エプロサルタン、テルミサルタンなど、このような環を持たない他のサルタン製剤は、今回のレビューには含まれていないが、後続の他の医薬品のレビューでカバーされている。
アジド化合物
2021年4月、欧州医薬品品質理事会(EDQM)は、テトラゾール含有サルタンに非ニトロソアミン系不純物(具体的にはアジド化合物)が混入するリスクがあることを警告した。2021年9月、EDQMは調査によりロサルタンのみに存在する新規のアジド系不純物(ロサルタンアジドまたはロサルタンアジド不純物)が発見され、エームス試験で変異原性が認められたと発表した。
その後、2021年と2022年にロサルタン、イルベサルタン、バルサルタンにアジド系不純物の混入が数例検出され、オーストラリア、ブラジル、欧州(スイスを含む)で調査から市場撤去、予防的回収に至る規制当局の対応が行われた。
Teva Pharmaceuticalsは、これらの不純物の混入を防ぐためにロサルタンの製造工程を変更すると発表し、インドの原薬メーカーであるIOLケミカルズ・アンド・ファーマシューティカルズは、アジド汚染物質を含まないように設計されたロサルタンの新しい合成に関する特許を申請した。
外部リンク
- Angiotensin II Type 1 Receptor Blockers at the U.S. National Library of Medicine Medical Subject Headings (MeSH)
- "Nitrosamine impurities in medications: Guidance". Health Canada. 4 April 2022.